북미·유럽 중심 구조 흔들리며 MRCT 다극화 본격화
한국 포함 아시아, 글로벌 임상 허브로 기회 확대
'LSK글로벌PS 창립 25주년 기념 심포지엄' 성료


|
다지역임상시험(Multi-Regional Clinical Trial, MRCT) 무게추가 이동하고 있다. 글로벌 신약개발 기업들이 오랫동안 임상 허가 시장으로 삼아온 북미와 유럽 중심 구조가 최근 몇 년 사이 크게 흔들리며, 중국과 아시아가 새로운 성장 축으로 부상하고 있다.

|
LSK글로벌PS 황세희 전무는 최근 서울 송파구 소피텔 앰배서더 서울에서 열린 ‘LSK글로벌PS 창립 25주년 기념 심포지엄’에서 "MRCT에서 국가 선정은 단순히 지리적 구분을 넘어 규제 환경, 산업적 가치, 환자 모집 여건까지 고려해야 하는 종합 전략"이라며 "특히 최근 중국과 아시아 태평양 지역의 참여 비중이 뚜렷하게 확대되고 있다"고 강조했다.
다지역임상시험은 하나의 임상시험 프로토콜(계획서)에 따라 두 개 이상의 국가 및 지역에서 동시에 수행되는 임상시험을 말한다. 환자군을 여러 지역에서 모집해 비교·분석함으로써 신약의 효과와 안전성을 글로벌 차원에서 입증할 수 있다.
황 전무 발표자료에 따르면, 글로벌 상위 10대 제약사의 임상 1상은 76.8%가 단일국가(Local study)로 진행됐다. 그러나 2상부터는 다지역 비중이 66.0%로 증가했다. 3상에서는 72.2%까지 확대됐다. 후기 임상으로 갈수록 다지역임상시험의 중요성이 커진다는 의미다.
가장 흔한 지역 조합은 북미와 유럽으로 5.2%를 차지했다. 이어 북미와 남아시아 4.7%, 북미·유럽·동아시아·동남아시아 혼합 조합 2.7%, 동아시아와 동남아시아 2.5% 순이다. 제약사들이 허가 가능성을 높이고 환자 모집 속도를 확보하기 위해 북미·유럽에 더해 아시아까지 임상 무대를 확장하는 추세다.
국내도 다지역임상시험은 꾸준히 증가하고 있다. 유한양행은 렉라자(레이저티닙)를 얀센과 함께 리브리반트(아미반타맙) 병용요법으로 북미·유럽·아시아에서 다지역임상을 수행했고, 2024년 FDA 승인을 획득했다.
또 삼성바이오에피스와 셀트리온은 바이오시밀러 글로벌 허가를 위해, 에이비엘바이오, 리가켐바이오사이언스, 알테오젠은 글로벌 파트너십을 기반으로 다지역임상시험을 진행 중이다.
중국, 단숨에 '3대 축'으로 부상
중국이 임상시험 데이터 신뢰성 강화, 정부 정책적 지원, 병원 네트워크 확충 등이 맞물리며 글로벌 임상 파트너로서 존재감을 키우고 있다.
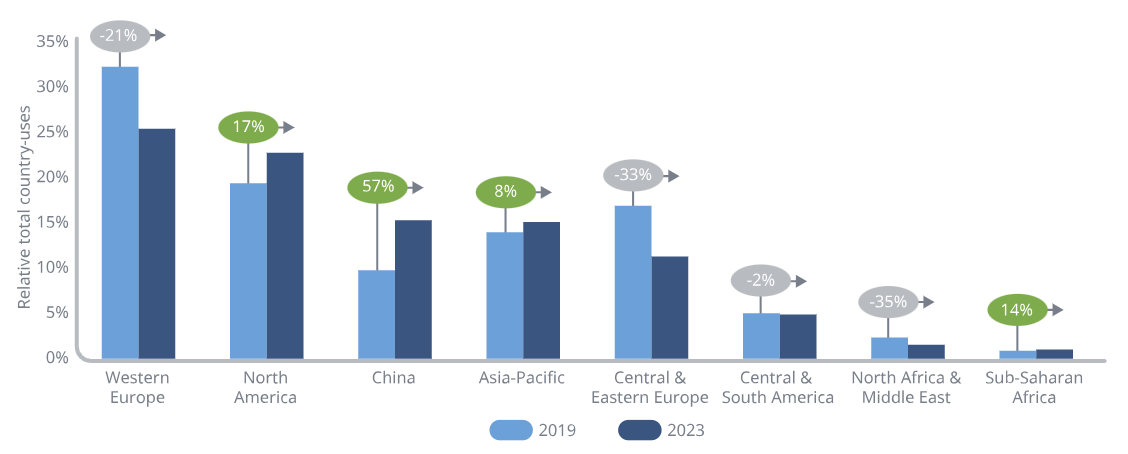
발표 자료에 따르면, 중국은 전체 임상시험 비중이 2019년 10%에서 2023년 15%로 5%p 상승(57% 증가)했다. 반대로 서유럽은 32%에서 25%로 7%p 하락(-21%)하며 여전히 가장 큰 비중을 차지하지만 하락세가 뚜렷했다. 중·동부 유럽도 17%에서 11%로 6%p 감소(-33%)하며 순위가 크게 밀렸다.
북미는 19%에서 23%로 4%p 확대(+17%)됐고, 아시아·태평양(중국 제외)은 12%에서 13%로 소폭 증가(+8%)했다. 이외에도 중남미는 5%에서 4%(-2%), 중동·북아프리카는 2%에서 1%(-35%), 사하라 이남 아프리카는 낮은 비중이지만 14% 증가세를 보였다. 아울러 한국은 2022년 전 세계 임상시험의 약 3.6%를 차지한 것으로 추정된 바 있다.
황 전무는 "중국의 임상시험 참여 건수와 비중은 불과 몇 년 사이 큰 폭으로 늘었다"며 "북미와 아시아 태평양 지역 역시 성장세를 이어가면서 글로벌 MRCT 구조가 다극화되고 있다"고 분석했다.
중국의 다지역임상시험 참여 확대는 단순한 숫자 증가를 넘어, 아시아 전체 임상시험 네트워크 강화와 신흥국 임상 데이터 가치 상승으로 이어지는 구조적 변화를 의미한다. 글로벌 빅파마들이 중국 내 환자 모집 속도와 정부 주도의 임상 인프라 확장을 주목하면서, 글로벌 임상 전략에서 빼놓을 수 없는 축으로 자리 잡은 것이다.
황 전무는 "중국과 아시아 태평양 지역의 임상시험 발전과 참여 증가는 아시아 지역 보건 의료 인프라 성장의 결과"라며 "MRCT 국가 선정은 단순한 지리적 구분이 아닌, 규제 환경, 산업적 가치, 환자 모집 여건까지 종합적으로 고려해야 한다"고 강조했다.
다지역임상시험에서 아시아 지역 참여가 확대되면서, CRO(임상시험수탁기관) 네트워크와 역량도 중요한 요소로 떠오르고 있다.
LSK글로벌PS는 현재 일본 MPI, 대만 StatPlus, 베트남 Horus, 태국 Aclires, 인도네시아 Equilab 등과 전략적 협력을 맺고 있다. 이를 통해 다지역임상에서 효율적인 환자 모집과 품질관리 기반을 확보했다.
황 전무는 “LSK글로벌PS는 한국을 허브로 아시아 네트워크를 확장하며, 임상 디자인부터 데이터 관리·규제 대응까지 MRCT 전 과정을 과학적·체계적으로 수행하고 있다"며 “특히 아시아 각국의 규제 경험과 글로벌 제약사와의 협업 노하우를 기반으로, 신속하면서도 표준화된 임상시험 플랫폼을 제공하는 것이 강점"이라고 전했다.
|
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











