뉴스
망막병증 치료제 '도베실산칼슘수화물' 성분 허가사항 변경
식약처, 안전성·유효성 심사 결과 면역계 장애 등 이상반응 추가
김용주 기자 │ yjkim@yakup.com


입력 2019-12-17 06:00 수정 2019.12.17 07:01
|
식품의약품안전처는 '도베실산칼슘수화물 함유제제(경구제)' 에 대하여 안전성·유효성 심사 등을 근거로 허가받은 4품목의 사용상의 주의사항을 통일조정할 예정이라고 밝혔다.
안전성·유효성 심사결과, 신부전,간부전 환자에게는 투여를 신중히 할 것을 사용상 주의사항에 반영하도록 했다.
도베실산칼슘수화물은 뇨를 통해 배설되므로 신부전 환자에게 투여 시 주의해야 하며, 특히 투석을 필요로 하는 중증 신부전 환자에게 이 약 투여용량을 감량할 수 있다는 내용을 반영하도록 했다.
또 간부전 환자에게는 유의한 간수치 상승이 나타날 경우 치료 유익성에 대한 재평가가 권고된다는 내용을 추가하도록 했다.
이와함께 이상반응으로 △혈액 및 림프계 장애(매우 드물게 : 무과립구증, 빈도 불명 : 호중구 감소증, 백혈구 감소증) △면역계 장애(흔하지 않게 : 피부 발진, 알러지성피부염, 가려움증, 두드러기, 얼굴부종, 매우 드물게 : 아나필락시스 반응) △신경계 장애(흔하게 : 두통) △위장관계 장애(흔하게 : 복통, 구역, 설사, 구토) 등을 추가하도록 했다.
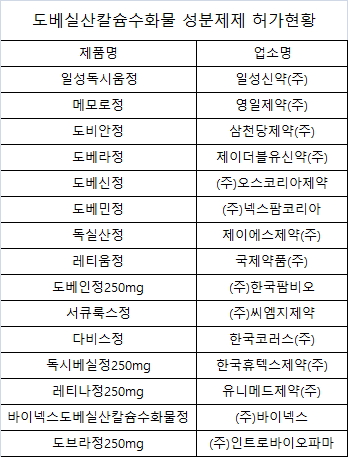
도베실산칼슘수화물의 일성신약의 '일성독시움정' 등 14품몰이 허가돼 있다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 삼원약품 창립 52주년 “2026년, 지역 최고 ... -
02 곽순헌 보건의료정책관 "간병비·PA 아우르는... -
03 한국유니온제약 상폐 수순…정리매매 돌입 속... -
04 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
05 에피바이오텍, 동종 모유두세포 치료제 핵심... -
06 트럼프,의약품 관세 부과...한국산 의약품 1... -
07 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
08 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
09 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
10 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ...











