뉴스
골격근이완제 '바클로펜' 성분제제 이상반응에 '자살' 추가
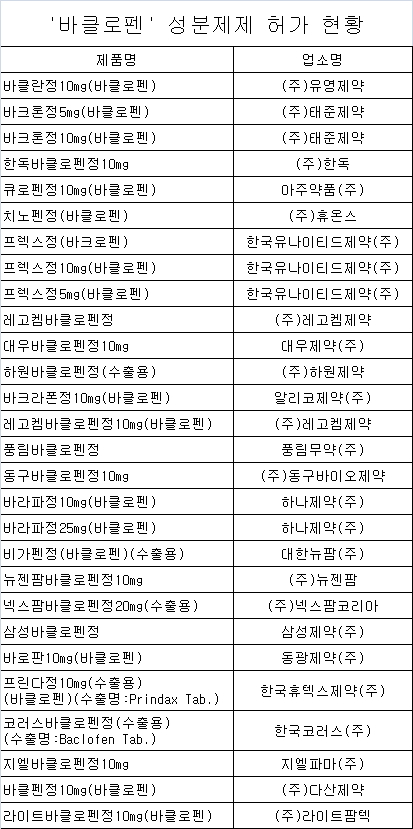
식약처, 휴온스 '치노펜정' 등 28품목 허가사항 변경
김용주 기자 │ yjkim@yakup.com


입력 2019-12-24 12:30 수정 2019.12.24 13:38
|
식품의약품안전처는 '바클로펜' 경구제의 안전성 정보와 관련해 국내·외 허가현황 등을 토대로 국내에서 허가받는 23개사 28품목에 대해 2020년 1월 23일자로 허가사항을 변경 지시했다고 밝혔다.
'바클로펜' 경구제는 허가사항중 일반적 주의사항에 "이 약으로 치료받은 환자에서 자살 및 자살관련 사례가 보고되었다. 대부분의 사례에서 환자에서 알코올 사용 질환, 우울증 및 이전에 자살 시도 이력을 포함한 자살의 위험성증가와 관련된다. 이 약 치료시 자살에 대한 추가 위험 요인이 있는 환자에 대해 면밀한 감독이 동반되어야 한다. 환자의 가족이나 보호자 또한 환자의 임상적 악화, 자살행동/생각 또는 비정상적인 기분과 행동의 변화에 대해 주의 깊게 관찰하고 이러한 증상 또는 행동이 발현될 경우 즉시 의료전문가에게 보고될 수 있도록 한다"는 내용을 추가하도록 했다.
또 "바클로펜과 관련하여 오용, 남용 및 의존사례가 보고되었다. 환자가 과거에 약물남용의 경험이 있는지를 확인해야 하고 약물 남용, 오용 및 의존하는 징후(예: 용량증가, 약물추구행동, 내성발현)가 있는지 세심하게 모니터링해야 한다"는 내용을 신섷하도록 했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











