
한국얀센의 '인보카나정 100mg' 등 당뇨병 치료제 'SGLT2 저해제'에 대한 시판후 조사에서 '회음부 괴저' 부작용이 발생한 것으로 보고돼 허가사항이 변경된다.
식품의약품안전처는 SGLT2 저해제의 안전성 정보와 관련해 국내외 허가현황 및 전문가 의견 등을 바탕으로 4월 6일자로 허가사항을 변경 지시했다고 밝혔다.
식약처는 "SGLT2 저해제를 복용한 당뇨병 환자의 시판 후 조사에서 드물기는 하나 신속한 수술적 중재를 필요로 하고, 생명을 위협하는 심각한 회음부 괴저가 보고되었다. 회음부 괴저는 남성과 여성 모두에서 보고되었으며 이로 인한 입원, 여러 차례의 수술 및 사망이 보고되었다'는 내용을 주의사항에 반영할 것을 지시했다.
또 " 이 약을 투여 받는 환자에서 발열 및 불편함과 함께 생식기 또는 회음부 주변의 통증, 짓무름, 홍반 또는 부종이 나타나는 경우 회음부 괴저 여부를 확인해야 한다. 회음부 괴저가 의심되는 경우, 즉시 광범위 항생제 치료를 시작하고 필요한 경우 외과적 절제술을 시행하여야 한다. 이 약의 투여를 중단하고 혈당 수치를 면밀히 모니터링하면서 혈당조절을 위한 적절한 대체 치료를 시행하여야 한다"는 내용도 추가했다.
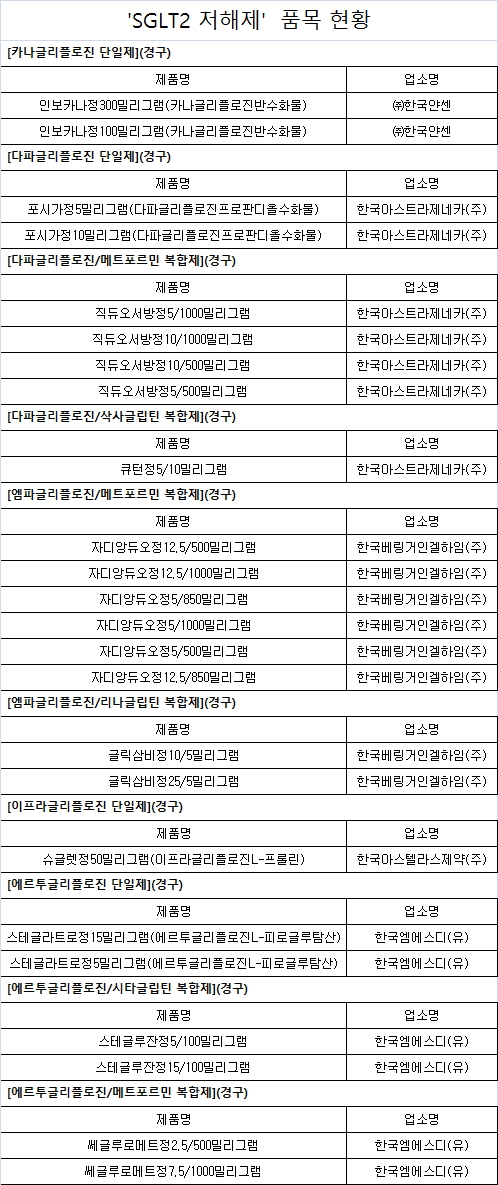
허가사항이 변경되는 당뇨병치료제 'SGLT2 저해제'는 △카나글리플로진 단일제(경구) 2품목 △다파글리플로진 단일제(경구) 2품목 △다파글리플로진/메트포르민 복합제(경구) 4품목 △다파글리플로진/삭사글립틴 복합제(경구) 1품목 △엠파글리플로진/메트포르민 복합제(경구) 6품목 △엠파글리플로진/리나글립틴 복합제(경구) 2품목 △이프라글리플로진 단일제(경구) 1품목 △에르투글리플로진 단일제(경구) 2품목 △에르투글리플로진/시타글립틴 복합제(경구) 2품목 △에르투글리플로진/메트포르민 복합제(경구) 2품목 등 10개 성분 24 품목이다.
|
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











