뉴스
"식약처, 부정확한 검토자료로 원료약 등록"
감사원 주요 취약분야 집중감찰…책임회피 위해 GMP 평가기준 번복도
이승덕 기자 │ duck4775@yakup.com


입력 2018-03-15 06:00 수정 2018.03.15 08:58
식약처가 제조기록서와 공정 밸리데이션 검토 자료 등이 부합하지 않는 자료를 기초로 원료약을 등록해 지적받았다.
이에 대해 감사원은 주의·통보 등 2건의 시정조치를 통해 식약처가 관련 업무를 철저히 하고, 평가자료를 규정에 맞지 않게 수정·변경한 중국 제조소 제조공정을 재검토할 것을 주문했다.

|
보고서 주요 내용을 보면, 식약처는 2015년 5월 6일 A사로부터 B에 대한 원료의약품 등록신청을 받아 이를 심사해 2016년 2월 17일 원료의약품으로 등록했다.
A는 B의 제조공정에 대해 중국에 소재한 C사(이하 중국 제조소)로부터 데옥시리보핵산트륨(Sodium Deoxyrbonucleic Acide, SDNA)을 수입해 A사의 한국 제조소에서 정제 등 공정을 거쳐 B를 제조한다는 내용의 관련 자료를 제출했다.
그런데 이번 감사에서 A사가 식약처에 제출한 GMP 평가자료를 검토한 결과, 중국 제조소가 기재한 도데실황산나트륨(Sodium Dodecyl Sulfate)의 질량과 농도가 각각 640g, 2.0%로 돼 있는데 제조기록서와 같은 공정을 대상으로 하는 공정 밸리데이션 검토자료에는 각각 640kg, 0.5%로 기재돼 있었다.
또한 시료번호 140603 제조기록서는 2014년 6월 16일부터 19일까지 생산된 것으로 기재돼 있지만, 제조기록서 작성일자는 제조기록서상 생산일자보다 빠른 6월 13일로 돼 있었으며, 시료번호 140603 시험성적서는 생산일자가 제조기록서에 기재된 생산일자(2014년 6월 16~19일)와 다른 2014년 6월 12일로 일치하지 않았다.
제조공정 순서에 있어서도 '시료 준비 및 장비 세척상태 확인' 공정이 '분쇄·가용화' 공정보다 앞서야 하나 제조기록서에는 후행 공정인 '분쇄·가용화' 공정이 선행 공정인 '시료 준비 및 장비 세척상태 확인' 공정일자(2014년 6월 16일)보다 빠른 6월 13일에 진행된 것으로 기재돼 있는 등 GMP 평가자료 신뢰성이 의심되는 사항들이 확인됐다.
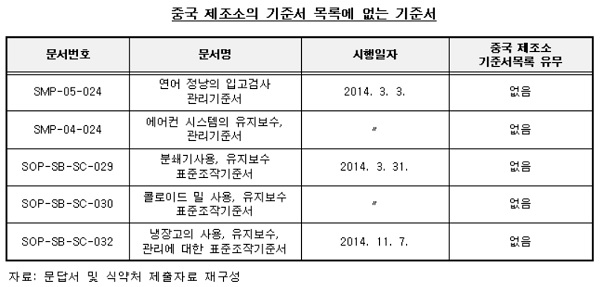
뿐만 아니라 A사가 제출한 중국 제조소의 기준서와 기준서 목록을 비교한 결과, A사는 중국 제조소 기준서 목록에 기재돼 있지 않은 문서번호 SMP-050024 '연어 넝낭의 입고검사 관리 기준서' 등 중국 제조소의 기준서 목록에 없는 5개 기준서를 제출한 것으로 확인됐다.
|
이와 관련 감사원이 A사의 원료의약품 등록 신청서류와 관련한 중국 제조소의 제조시설 관련 자료, 제조기록 등을 통해 업무처리과정을 추가 확인한 결과, 중국 제조소의 SDNA 제조공정 등 실시상황이 의약품 제조 및 품질관리 기준에 맞는지 여부를 평가하는데 있어 관련 규정에 따른 절차를 거치지 않고 수정·변경됐다.
구체적으로는 A사가 제조기록서에 착오 또는 계산상 오류가 있다는 이유로 2015년 12월 22일 제조기록서에 기재된 도데실황산나트륨 농도를 0.5%에서 2.0%로 수정했으며, 2015년 12월부터 2016년 1월 8일까지 중국 제조소를 통해 제조기록서를 수정하면서 GMP 평가 기준에 따라 수정하려는 글자 또는 문장의 수정 전 상태를 알아볼 수 있게 선을 긋거나 수정 사유, 연월일 및 수정자의 서명을 표기하지 않은 채 제조지시 내용 자체를 수정했다.
또한 A사가 2015년 11월경 중국 제조소로부터 전달받은 제조기록서와 식약처에 최종 제출한 제조기록서를 비교한 결과, 제조기록서 지시 내용 중 도데실황산나트륨 농도와 질량 등이 수정된 외에도 수기로 기입하는 부분의 필체도 달라지는 등 A사는 수정이력을 남기지 않은 채 특정 쪽을 교체한 제조기록서를 2016년 1월 8일 식약처에 최종 제출한 것으로 판단됐다.
식약처가 2016년 1월 19일 추출 공정에 대한 공정 밸리데이션 검토자료 등 추가자료의 보완을 요구하자, A사는 중국 제조소로부터 수입하는 SDNA 시료 140601, 140602,140603의 공정 밸리데이션 보고서 초안을 2016년 1월 8일 식약처에 제출한 제조기록서 등을 토대로 작성하고 2016년 1월 25일 이를 중국어로 번역하고 중국 제조소에 보낸 후 2016년 2월 5일 공정 밸리데이션 보고서 초안과 주요 내용이 동일한 보고서를 식약처에 제출했다.
감사원은 "A사로부터 관련 규정에 맞지 않게 수정·변경된 제조기록서와 이를 기초로 작성된 공정 밸리데이션 자료 등을 제출받아 GMP 평가기준의 적합 여부가 심사됐다"며 "이 때문에 중국 제조소에서 제조 및 시험이 실제 어떻게 진행됐는지, 그리고 2014년 SDNA 제조 당시 제조공정에서 미리 설정된 기준과 품질 특성에 맞는 제품을 일관되게 제조한다는 것이 검증됐는지 제대로 확인됐다고 보기 어렵다"고 평가했다.
이에 대해 식약처는 A사가 중국 제조소로부터 수입한 SDNA는 원료의약품 B의 출발물질에 불과해 '그 자체가 약리 활성을 가진 물질로 화학적 기본구조의 변화 없이 단순히 순도를 높이기 위한 정제공정이나 결정화공정 등 처리공정을 거쳐 최종 원료의약품이 되는 상태의 원료'인 조품(Crude)로 볼 수 없기 때문에 SDNA는 의약품 제조 및 품질관리기준에 적합하게 제조됐는지를 평가할 대상이 아니라고 밝혔다.
A사는 중국 제조소와 언어의 장벽으로 인한 업무 처리 절차 등에 관해 협의하는 과정에서 관련 서류의 오기를 수정한 것이라고 하면서 식약처가 관계 규정에 맞게 검토해 업무를 처리했다고 주장하고 있다.
그러나 감사원은 "식약처는 2015년 11월 25일 A사에 SDNA를 조품이라고 기재하면서 조품 제조소의 시설 관련 자료 및 GMP 증명서 등 관련자료를 제출하도록 요구한 바 있고, 2016년 2월 17일 A사의 원료의약품 등록을 검토하면서 작성한 '원료의약품 등록 신청서 검토서'에도 중국 제조소를 조품 제조소라고 명시하고 있고, 같은 날 A사의 원료의약품 등록을 승인하면서도 중국 제조소를 소품 제조소로 명시해 소재지까지 기재했다"고 짚었다.
이어 "이 건과 관련해 주식회사 C사가 2016년 3월 29일 감사원에 요청한 심사청구에 대해 식약처가 제출한 의견서에도 '원료의약품의 조품 제조원(C사, 중국)'으로 표기하고 있는 등 그동안 식약처 업무처리 입장과 배치된다"고 지적했다.
감사원은 또 "A사가 식약처 GMP 관련 보완자료 요청에 대해 수입대상 물품은 조품이 아닌 원료의약품의 '출발물질'에 불과하다며 GMP 평가대상이 아니라고 이의신청했으나, 식약처는 출발물질의 투입 이후단계부터는 '원료의약품 제조 및 품질관리에 관한 기준 가이던스'가 적용된다며 '냉동된 연어 어정의 해동'단계부터는 GMP 평가범위에 명백히 해당된다는 내용으로 회신한 바도 있다"고 함께 언급했다.
특히 "식약처는 2015년 11월 경 내부 회의를 통해 SDNA를 GMP 평가기준에 따라 평가하기로 했으므로, SDNA의 조품 해당여부를 떠나 위 방침에 따라 관련 규정 준수 여부를 검토해야 했다"며 "실제 식약처는 GMP 평가기준에 따라 관련규정 준수여부를 검토한 사실이 있었는데도 감사에서 지적되자, 당초 입장을 번복해 조품이 아니라 GMP 평가대상이 아니라고 주장하는 것은 책임을 면하려는 변명으로 보인다"고 질타했다.
한편, 감사원은 전문연구기관 자문 결과를 근거로 중국 제조소로부터 수입하는 SDNA가 그 자체로 약리활성을 가진 물질이기 때문에 식약처의 GMP 평가대상이 아니라는 주장을 받아들이기 어렵다고 첨언하기도 했다.
감사원은 '주의' 조치를 통해 식약처장이 앞으로 제조기록서와 공정 밸리데이션 검토자료 등이 불부합하는 등 사실관계가 의심되는 평가자료를 기초로 심사해 원료의약품으로 등록하는 일이 없도록 관련 업무를 철저히 하도록 했다.
더불어 '통보' 조치로 원료의약품 등록 심사를 위한 평가자료를 관련 규정에 맞지 않게 수정·변경해 제출한 A사의 데옥시리보핵산나트륨 제조소인 C사의 제조공정 등에 대해 '의약품 등 품목별 사전 GMP 평가 운영 지침'에 따라 실태조사 등을 통해 '의약품 등의 안전에 관한 규칙'의 별표 '의약품 제조 및 품질관리 기준'에 적합한지 여부를 재검토하는 방안을 강구하라고 주문했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











