dMMR·MSI-H 진행성 위선암·위식도접합부 선암 대상 면역항암제 급여범위 확대

|
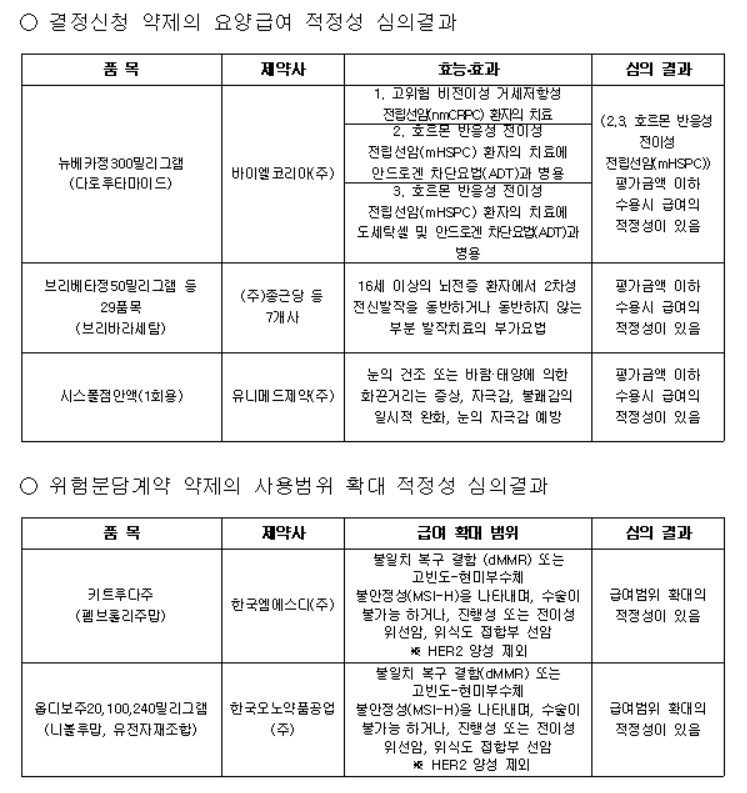
전립선암 치료제 ‘뉴베카’가 호르몬 반응성 전이성 전립선암 적응증에서 조건부로 급여 적정성을 인정받았고, 면역항암제 ‘키트루다’와 ‘옵디보’는 위암 치료에서 급여범위 확대의 적정성이 인정됐다.
건강보험심사평가원(원장 강중구)은 5일 2026년 제3차 약제급여평가위원회에서 심의한 약제 급여 적정성 평가 결과를 공개했다.
이번 심의에서 바이엘코리아의 전립선암 치료제 뉴베카정 300밀리그램(다로루타마이드)은 호르몬 반응성 전이성 전립선암(mHSPC) 환자의 치료에서 안드로겐 차단요법(ADT) 병용 또는 도세탁셀 및 ADT 병용요법에 대해 제약사가 평가금액 이하를 수용할 경우 급여의 적정성이 있다고 판단됐다.
뉴베카는 안드로겐 수용체 억제제 계열 전립선암 치료제로, 전이됐지만 호르몬 치료에 반응하는 호르몬 반응성 전이성 전립선암(mHSPC) 환자에서 안드로겐 차단요법 또는 도세탁셀 병용요법으로 사용되는 치료제다.
또 종근당 등 7개사가 신청한 브리베타정 50밀리그램 등 브리바라세탐 성분 29품목은 ‘16세 이상의 뇌전증 환자에서 2차성 전신발작을 동반하거나 동반하지 않는 부분 발작 치료의 부가요법’ 적응증으로 급여 평가를 받았으며, 평가금액 이하 수용 시 급여 적정성이 인정됐다.
브리바라세탐은 뇌전증 치료에 사용되는 SV2A 결합 항경련제로, 부분 발작 환자에서 기존 항경련제 치료에 추가하는 부가요법으로 사용된다.
유니메드제약의 시스폴점안액(1회용)도 ‘눈의 건조 또는 바람·태양에 의한 화끈거림, 자극감, 불쾌감의 일시적 완화 및 눈 자극감 예방’ 적응증에 대해 평가금액 이하 수용 시 급여 적정성이 인정됐다.
이와 함께 약평위는 위험분담계약(RSA) 약제의 사용범위 확대 적정성도 심의했다.
그 결과 한국MSD의 키트루다주(펨브롤리주맙)와 한국오노약품공업의 옵디보주(니볼루맙)는 불일치 복구 결함(dMMR) 또는 고빈도 현미부수체 불안정성(MSI-H)을 나타내며 수술이 불가능하거나 진행성 또는 전이성 위선암·위식도접합부 선암 환자(HER2 양성 제외)에 대해 급여범위 확대의 적정성이 인정됐다.
dMMR 또는 MSI-H 종양은 DNA 복구 기능 결함으로 인해 돌연변이 부담이 높은 종양으로, 면역항암제 반응률이 높은 것으로 알려져 있다.
한편 약평위를 통과한 약제는 국민건강보험공단과 최대 60일간 약가 협상을 진행한 뒤 건강보험정책심의위원회 심의를 통해 최종 급여 여부가 결정된다.
-
01 오젬픽 광고, FDA 검토 대상 올라 -
02 동국제약, 지난해 영업이익 20% 급증… 매출 ... -
03 보건의료 난제 풀 ‘한국형 ARPA-H’, 2026년 ... -
04 테바, 세계적 민간투자사서 개발비 4억 달러... -
05 '전문경영인 체제' 두고 쪼개진 한미 4자 연... -
06 중동 하늘길·바닷길 막히나... 화장품 업계 ... -
07 [인터뷰] "K-뷰티, 제품이 아니라 '아카이브... -
08 뉴베카 전립선암 조건부 급여 적정성…키트루... -
09 싱귤래리티바이오텍 “344개 유전자변이 망막... -
10 안지오랩 “ALS-L1023, 주사 중심 황반변성에...











