신약 다수는 급여기준 미설정…자카비·포말리스트 등은 확대

|
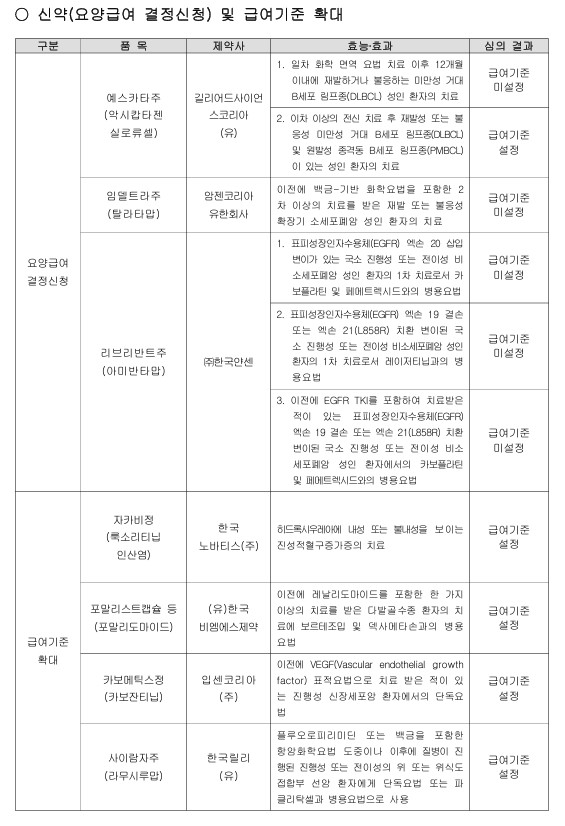
2026년 첫 중증(암)질환심의위원회에서 신약 항암제들의 급여 향방이 엇갈렸다. 신규 등재를 노린 항암 신약 다수는 급여기준을 설정하지 못했고, 이미 급여 중인 약제를 중심으로 적응증 확대가 이뤄졌다.
CAR-T 치료제 예스카타는 적응증에 따라 일부 급여기준이 설정된 반면, 리브리반트와 임델트라 등 주요 신약은 급여기준이 미설정되며 문턱을 넘지 못했다.
건강보험심사평가원은 21일 2026년 제1차 암질환심의위원회 심의 결과를 공개했다. 올해 처음 열린 이번 회의에서는 신약 요양급여 결정신청 안건과 기존 항암제의 급여기준 확대 여부가 함께 논의됐다.
△예스카타, 2차 이상 DLBCL·PMBCL서 급여기준 설정
길리어드사이언스코리아의 CAR-T 치료제 예스카타주(악시캅타젠 실로류셀)는 적응증별로 상이한 결과를 받았다.
‘일차 화학면역요법 치료 이후 12개월 이내 재발하거나 불응한 미만성 거대 B세포 림프종(DLBCL)’ 적응증에 대해서는 급여기준이 설정되지 않았다.
반면, 이차 이상의 전신 치료 후 재발성 또는 불응성 DLBCL 및 원발성 종격동 B세포 림프종(PMBCL) 성인 환자 치료에 대해서는 급여기준이 설정됐다.
이에 따라 예스카타는 일부 고위험 환자군에서 급여기준이 설정됐으며, 조기 재발 환자군에 대해서는 급여기준이 마련되지 않았다.
△임델트라·리브리반트, 상정 적응증 모두 ‘미설정’
암젠코리아의 임델트라주(탈라타맙)는 백금 기반 화학요법을 포함한 2차 이상 치료를 받은 재발·불응성 확장기 소세포폐암 성인 환자 치료를 적응증으로 심의에 올랐으나, 급여기준이 설정되지 않았다.
한국얀센의 리브리반트주(아미반타맙) 역시 상정된 모든 적응증에서 급여기준이 미설정됐다.
리브리반트는 △EGFR 엑손 20 삽입 변이 비소세포폐암 1차 치료 병용요법 △EGFR 엑손 19 결손 또는 엑손 21(L858R) 치환 변이 환자의 1차 치료에서 레이저티닙 병용요법 △EGFR TKI 치료 경험 환자 대상 병용요법 등으로 급여기준 설정을 신청했지만 모두 받아들여지지 않았다.
△자카비·포말리스트·카보메틱스·사이람자 급여기준 확대
기존 항암제의 급여기준 확대 안건은 다수 통과됐다.
한국노바티스의 자카비정(룩소리티닙)은 히드록시우레아에 내성 또는 불내성을 보이는 진성적혈구증가증 치료에 대해 급여기준이 설정됐다.
한국비엠에스제약의 포말리스트캡슐(포말리도마이드)은 레날리도마이드를 포함한 한 가지 이상 치료를 받은 다발골수종 환자에서 보르테조밉·덱사메타손 병용요법으로 급여기준이 확대됐다.
입센코리아의 카보메틱스정(카보잔티닙)은 VEGF 표적요법 치료 경험이 있는 진행성 신장세포암 환자 단독요법에 대해 급여기준이 설정됐으며, 한국릴리의 사이람자주(라무시루맙) 역시 위 또는 위식도접합부 선암 환자에서 단독 또는 파클리탁셀 병용요법으로 급여기준이 마련됐다.
-
01 USP "GLP-1 비만치료제, 전쟁 승부처는 불순... -
02 뚫기 더 어려워진 '아마존'에서의 성공 전략은? -
03 향, 첫인상에 작동하는 ‘맥락 변수’ -
04 노보노디스크, 당뇨병 근치요법제 개발 도전장 -
05 조관구 지씨씨엘 대표 "바이오 투자 양극화 ... -
06 상장 제약바이오 2025년 3Q 평균 이자비용 ·... -
07 올해 첫 암질심, 예스카타 '부분 통과'…리브... -
08 그린란드 트럼프 관세 카드…의약품도 안전지... -
09 정맥에서 피하로…GSK, 젬펄리 제형 전략 가속 -
10 [2026 R&D⑧]산업통상부, 제약바이오 ‘제조 ...











