뉴스
“中 허가특허연계제도 통한 특허분쟁 대비해야”
‘시판의약품 특허정보 등록 플랫폼’ 전략 수립 등 적극 활용
김정일 기자 │ jikim@yakup.com


입력 2021-10-26 11:26
국내 제약사들이 중국 허가특허연계제도 시행과 연계해 의약품특허침해에 적극적으로 대응해야 한다는 제언이다.
한국지식재산연구원에 따르면 국내 제약회사들의 중국 진출이 활발한 만큼 중국에서 의약품 관련 특허분쟁도 증가할 것으로 예상하면서 중국 정부가 지난 6월 1일부터 시행한 허가특허연계제도의 이해와 함께 이 제도를 통한 특허분쟁 발생 가능성에 대비할 필요가 있다.
중국은 지난 7월 4일부터 중국에서 시판승인을 받은 의약품의 특허정보가 수록된 데이터베이스인 ‘시판의약품 특허정보 등록 플랫폼’(https://zldj.cde.org.cn)을 운영하고 있다. 중국에서 의약품의 시판 허가를 받은 제약사는 “시판 의약품 특허정보 등록 플랫폼”에 의약품의 명칭, 시판허가를 받은 자, 제형, 관련 특허명칭, 특허번호, 특허존속기간 등을 공개해야 하며, 관련 정보가 변경되는 경우에도 이를 업데이트해야 한다.
시판의약품 특허로서 이 플랫폼에 등록하는 것은 의약품 허가특허연계제도의 적용 대상이 되는 특허를 결정하는 단계라는 점에서 의의를 가진다는 설명이다.
만일 제네릭의약품을 만들어 시판승인 신청을 하는 경우에는 ‘시판의약품 특허정보 등록 플랫폼’에 등록된 특허와의 관계를 허가 당국에 설명(선언)해야만 한다. 선언에는 4가지 종류가 있는데 ▲시판의약품 특허정보 등록 플랫폼에는 제넥릭의약품과 관련된 특허정보가 존재하지 않는다거나 ▲관련 특허권이 만료 또는 무효로 됐다거나 ▲관련 특허권이 존재하나 특허만료 전까지는 시판하지 않겠다거나 ▲관련 특허권에 무효사유가 있어 무효화돼야 하고 제네릭의약품은 특허권의 보호범위에 속하지 않는다는 선언 중 하나를 선택해야 한다.
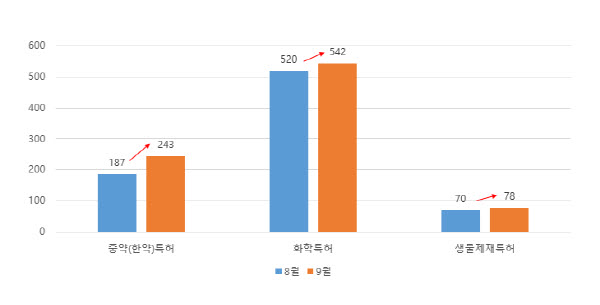
2021년 9월 현재까지 이 플랫폼에는 중약특허 243건, 화학의약품특허 542건, 바이오의약품특허 78건으로 총 863건의 의약품특허 목록이 공개돼 있다. 또한 이 플랫폼에서는 시판승인신청 의약품이 관련 특허를 침해하지 않는다는 선언서(Certification)를 검색할 수도 있다.
|
한국지식재산연구원 이명희 박사는 “최근 중국 의약품 시장 진출이 활발한 우리나라 제약사는 중국의 제도 변화에 보다 세심한 관심을 기울일 필요가 있다”며 “시판의약품 특허정보를 반드시 등록하고 이미 등록된 정보를 적절히 활용해 중국 의약품 시장 진출을 위한 전략 수립이나 특허분쟁 방지 및 조기 해결에 만전을 기할 필요가 있다”고 밝혔다.
또한 “정부도 중국의 관련 제도 및 지침에 대한 적기의 분석을 통해 제약산업이 혼동이나 불이익을 입지 많도록 지원해야 할 것”이라고 덧붙였다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 한미약품, 미국암연구학회서 국내 최다 연구... -
02 [약업 분석] 코오롱생명과학, 적자 늪 벗어... -
03 유전자교정협의회 "한국 규제, 글로벌과 불... -
04 롯데바이오로직스, 일본 제약사와 항암 항체... -
05 SK바이오팜, AACR서 방사성의약품 성과 공개... -
06 SK바이오사이언스, 연구지원 조직 정비-핵심... -
07 셀트리온, 미국 의약품관세 영향 해소..현지... -
08 석정호 대표 "우울증 조기진단,자살위험 낮... -
09 소비자 기호 맞춘 제형 다변화…판피린 ‘국민... -
10 중동 변수 덮친 글로벌 뷰티업계…볼로냐서도...











