FH결핍 신장암·전립선암 일부 기준 확대…약평위·약가협상 거쳐 최종 결정

|
재발·불응성 혈액암과 전이성 대장암 치료 신약 2종이 건강보험 급여 등재를 위한 첫 관문을 통과했다.
건강보험심사평가원(원장 강중구)은 4일 열린 2026년 제2차 중증(암)질환심의위원회에서 심의한 ‘암환자에게 사용되는 약제 급여기준 심의결과’를 공개했다.
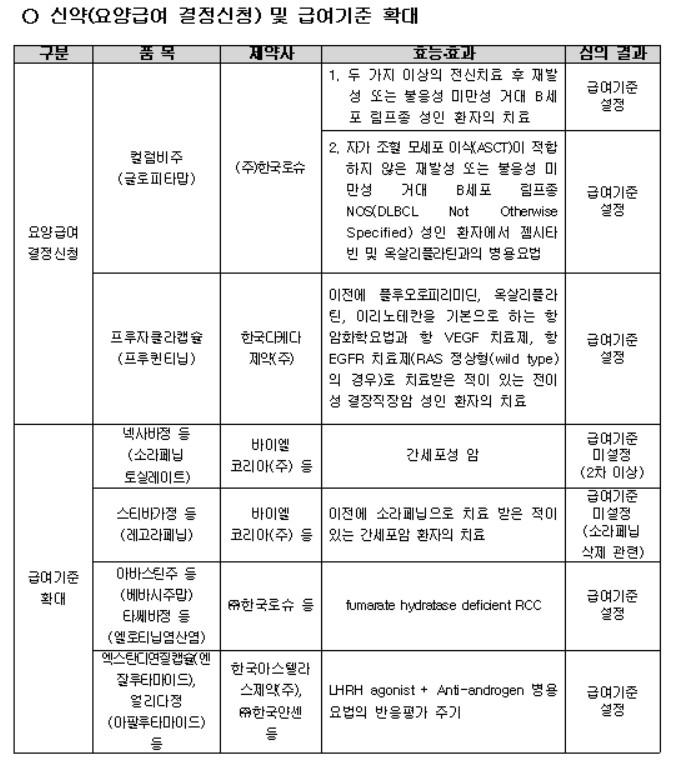
이번 심의에서는 한국로슈의 혈액암 치료제 ‘컬럼비주(성분명 글로피타맙)’와 한국다케다제약의 전이성 결장직장암 치료제 ‘프루자클라캡슐(성분명 프루퀸티닙)’의 급여기준이 설정됐다.
컬럼비는 두 가지 이상의 전신치료 후 재발하거나 불응한 미만성 거대 B세포 림프종(DLBCL) 성인 환자 치료에 대해 급여기준이 마련됐다. 또한 자가 조혈모세포 이식(ASCT)이 적합하지 않은 재발성 또는 불응성 DLBCL 환자에서 젬시타빈·옥살리플라틴 병용요법에도 급여 적용 기준이 설정됐다.
글로피타맙은 B세포 림프종 치료 분야의 이중특이항체 치료제로, 종양세포와 T세포를 동시에 결합해 면역 반응을 유도하는 기전을 가진다. 재발·불응성 DLBCL 치료에서 글로벌 가이드라인에서도 주요 치료 옵션으로 권고되고 있다.
전이성 결장직장암 치료제 프루자클라(프루퀸티닙) 역시 급여기준 설정 대상에 포함됐다. 해당 약제는 플루오로피리미딘·옥살리플라틴·이리노테칸 기반 항암화학요법과 항 VEGF 치료제, 항 EGFR 치료제(RAS 정상형의 경우) 치료 경험이 있는 전이성 결장직장암 성인 환자 치료에 사용할 수 있도록 했다.
프루퀸티닙은 혈관내피성장인자 수용체(VEGFR)를 선택적으로 억제하는 경구용 표적항암제로, 기존 치료 이후 사용되는 후기 치료 옵션으로 평가된다.
반면 간암 치료 영역에서는 급여 확대가 받아들여지지 않았다.
바이엘코리아의 ‘넥사바정(성분명 소라페닙)’은 간세포암 2차 이상 치료에 대한 급여기준 확대를 신청했지만 이번 심의에서 인정되지 않았다. 소라페닙은 그동안 간세포암 1차 치료 표준요법으로 사용돼 온 약제다.
또한 ‘스티바가정(성분명 레고라페닙)’ 역시 소라페닙 치료 경험 간세포암 환자 치료 관련 급여기준 변경이 논의됐지만 최종적으로 받아들여지지 않았다.
이와 함께 일부 약제의 급여기준 확대도 이뤄졌다.
아바스틴주(베바시주맙)과 타쎄바정(엘로티닙) 병용요법은 FH 결핍 신세포암(fumarate hydratase-deficient RCC)에 대해 급여기준이 설정됐다. FH 결핍 신세포암은 대사 효소 결핍과 관련된 희귀 신장암 아형이다.
또한 엑스탄디연질캡슐(엔잘루타마이드)과 얼리다정(아팔루타마이드) 등 전립선암 치료제의 경우 LHRH agonist와 항안드로겐 병용요법의 반응평가 주기에 대한 급여기준이 마련됐다.
한편 암질환심의위원회를 통과한 약제는 약제급여평가위원회의 경제성 평가와 국민건강보험공단과의 약가 협상을 거쳐 건강보험정책심의위원회에서 최종 급여 여부가 결정된다.
-
01 한국바이오협회,회원사 맞춤형 역량강화 실... -
02 미국 진출, 철저한 규제 준수와 준비 필요 -
03 FDA, GLP-1 제제 불법 마케팅 업체들에 경고문 -
04 복지부 이관 앞둔 국립대병원 …742억 인프라... -
05 커지는 희귀질환 시장… 희귀질환 치료제 확... -
06 화이자 CEO “FDA CBER 리더십 문제 있다” 공... -
07 사노피, 중국 시노바이오팜 신약에 15억달러... -
08 K-뷰티 구조적 성장 진행 중…2029년 150억 ... -
09 자동차보험 진료비 논의…"비용 통제보다 환... -
10 컬럼비·프루자클라 암질심 통과…넥사바·스티...











