리브리반트 일부 설정·다수는 보류…아이클루시그 신규 ALL 치료제 급여 불발

|
건강보험심사평가원(원장 강중구)은 3일 2025년도 제7차 암질환심의위원회를 열고 항암제 급여기준 신설 및 확대 여부를 심의한 결과를 공개했다.
이번 회의에서는 △레테브모캡슐(한국릴리) △리브리반트주(한국얀센) △린파자정(한국아스트라제네카) △아이클루시그정(한국오츠카제약) 등이 주요 안건으로 논의됐다.
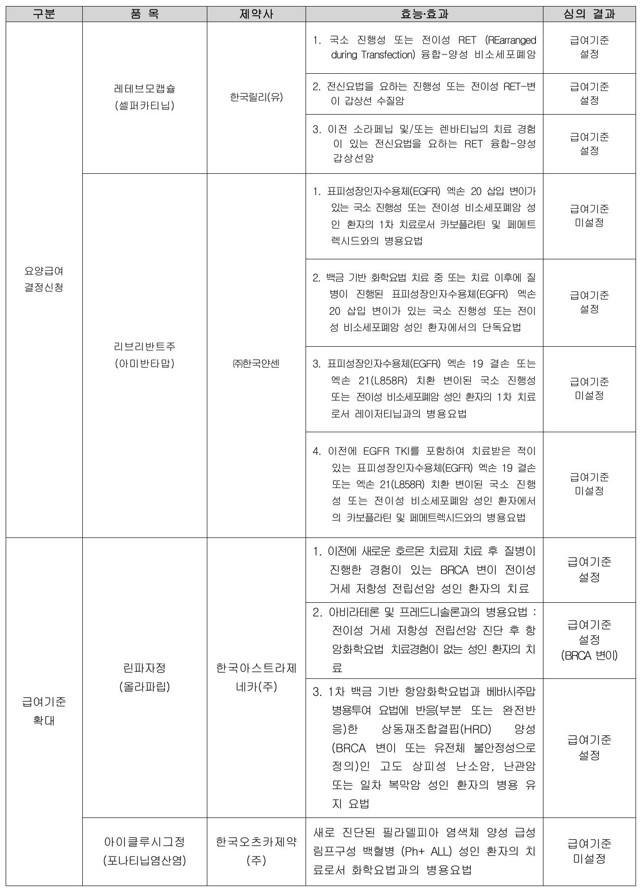
레테브모캡슐은 ▲국소 진행성 또는 전이성 RET (REarranged during Transfection) 융합-양성 비소세포폐암 ▲전신요법을 요하는 진행성 또는 전이성 RET-변이 갑상선 수질암 ▲이전 소라페닙 및/또는 렌바티닙의 치료 경험이 있는 전신요법을 요하는 RET 융합-양성 갑상선암 등 세 적응증 모두에서 급여기준이 신설됐다. 이에 따라 특정 바이오마커 기반 정밀항암제의 접근성이 한층 확대될 전망이다.
린파자는 ▲이전에 새로운 호르몬 치료제 치료 후 질병이 진행한 경험이 있는 BRCA 변이 전이성 거세 저항성 전립선암 성인 환자의 치료 ▲아비라테론 및 프레드니솔론과의 병용요법 : 전이성 거세 저항성 전립선암 진단 후 항암화학요법 치료경험이 없는 성인 환자의 치료 ▲ 1차 백금 기반 항암화학요법과 베바시주맙 병용투여 요법에 반응(부분 또는 완전반응)한 상동재조합결핍(HRD) 양성(BRCA 변이 또는 유전체 불안정성으로 정의)인 고도 상피성 난소암, 난관암 또는 일차 복막암 성인 환자의 병용 유지 요법에서 급여기준이 새로 마련됐다. 특히 기존 적응증 대비 확대 적용이 가능해지면서 환자 선택권이 넓어졌다는 평가다.
반면 리브리반트주는 백금 기반 화학요법 치료 중 또는 치료 이후에 질병이 진행된 표피성장인자수용체(EGFR) 엑손 20 삽입 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 성인 환자에서의 단독요법에서만 급여기준이 설정됐으며, 다른 병용요법 적응증은 모두 보류됐다.
아이클루시그정은 새로 진단된 Ph+ 급성림프구성백혈병(ALL) 치료제로 신청됐으나 급여기준은 설정되지 않았다.
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











