
|
이렇게 끝낼 순 없어?
FDA가 ‘소아 희귀질환 치료제 지정’(RPDD: Rare Pediatric Disease Disignation) 프로그램을 지난해 말 폐지한 이후 논란이 고개를 들고 있는 것으로 나타났다.
‘신속심사’나 ‘패스트 트랙’ 지정제도와 마찬가지로 개발‧심사과정에서 각종 인센티브를 제공하는 ‘소아 희귀질환 치료제 지정’ 프로그램이 도입된 후 허가를 취득하는 소아 희귀질환 치료제들이 급증한 것으로 나타난 바 있기 때문.
영국 런던에 소재한 비즈니스 정보 서비스업체 글로벌데이터社는 21일 공개한 자료에서 지난 2016년부터 2024년에 이르는 기간 동안 ‘소아 희귀질환 치료제 지정’ 건수에서 나타난 긍정적인 트렌드가 소아 희귀질환 치료제들의 허가건수 증가로 이어지면서 오롯이 반영됐다고 강조했다.
이 같은 분석결과는 ‘소아 희귀질환 치료제 지정’ 프로그램의 시행이 소아 희귀질환 치료제 시장에 긍정적인 영향을 미쳤음을 시사하는 것이라고 글로벌데이터는 풀이했다.
글로벌데이터 측에 따르면 소아 희귀질환은 환자 수가 적은 데다 금전적인 인센티브마저 제한적이어서 역사적으로 볼 때 신약개발에서 소외되어 왔던 분야이다.
이에 FDA는 지난 2012년 7월 ‘소아 희귀질환 치료제 지정’ 프로그램을 도입했다.
이 프로그램은 주로 18세 미만의 소아환자들에게 영향을 미치고 있는 희귀‧중증질환 치료제로 개발 중인 기대주들을 대상으로 엄격한 심사를 거쳐 지위를 부여해 왔다.
소아질환 치료제들을 개발하고 있는 제약기업들에게 금전적인 인센티브를 제공하고자 했던 것.
덕분에 소아 희귀질환 치료제가 허가를 취득할 경우 해당 제약사는 ‘신속심사’ 바우처 1매를 부여받을 수 있게 됐다.
이 ‘신속심사’ 바우처는 미래의 신약에 대한 FDA의 심사과정을 간소화하고 심사절차상의 우선순위를 부여하는 등 쏠쏠한 인센티브로 유용하게 활용됐다.
또는 바우처를 최대 3억5,000만 달러를 받고 판매할 수도 있도록 허용됐다.
하지만 의회는 이 제도의 효과에 의문을 표시하고 프로그램을 개정하지 않더니 지난해 말 폐지하는 결정을 내렸다.
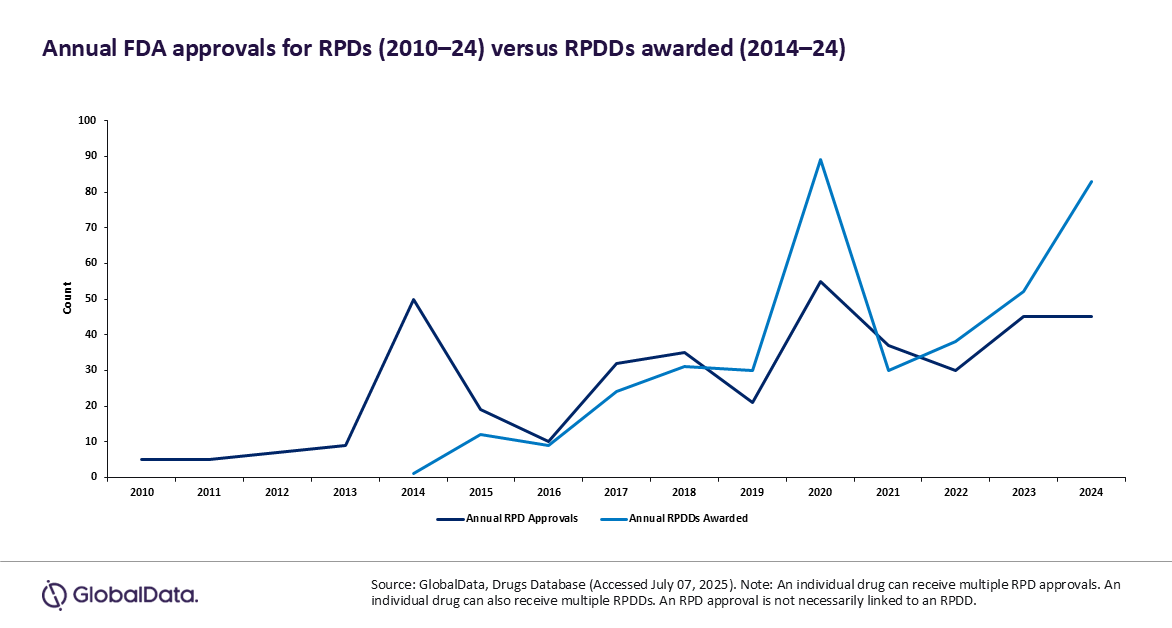
글로벌데이터 측에 따르면 지난 2010년부터 2013년에 이르는 기간 동안 매년 FDA의 허가를 취득한 소아 희귀질환 치료제는 연평균 6.5개로 나타나 상대적으로 낮은 수치를 유지했다.
글로벌데이터社의 재스퍼 몰리 제약산업 담당 애널리스트는 “FDA가 ‘소아 희귀질환 치료제 지정’ 프로그램을 시행하기 시작한 지난 2014년에 총 50개의 소아 희귀질환 치료제들이 허가관문을 통과해 2013년과 비교했을 때 5배나 높은 수치를 기록했다”고 강조했다.
하지만 2014년에 소아 희귀질환 치료제로 허가를 취득한 50개 신약들 가운데 ‘소아 희귀질환 치료제 지정’ 프로그램과 연계되었던 것은 1개에 불과했다고 지적했다.
바꿔 말하면 2014년에 소아 희귀질환 치료제들의 허가건수가 급증한 것은 ‘소아 희귀질환 치료제 지정’ 프로그램의 직접적인 영향이었다기보다 소아질환 전체에 우선순위를 두었던 FDA의 좀 더 폭넓은 이니셔티브에 기인한 성과였다는 설명이다.
그 후 2016년에 들어서는 10개의 소아 희귀질환 치료제들이 FDA의 허가를 취득한 것으로 나타났다.
몰리 애널리스트는 뒤이어 “2016~2024년 기간 동안 소아 희귀질환 치료제들의 허가에 전반적으로 긍정적인 트렌드가 눈에 띄었다”고 분석했다.
이 기간 동안 소아 희귀질환 치료제들의 FDA 허가건수가 연평균 16.2% 증가했기 때문이라는 것이다.
몰리 애널리스트에 따르면 소아 희귀질환 치료제들의 허가가 절정에 도달한 시점은 지난 2020년이어서 FDA가 무려 55개 치료제들을 승인한 것으로 나타났다.
같은 기간(2016~2024년) 동안 FDA로부터 ‘소아 희귀질환 치료제 지정’ 프로그램의 적용대상으로 지정된 건수를 보더라도 연평균 24.9% 증가하는 유사하고 긍정적인 추이가 눈길을 끌었다.
‘소아 희귀질환 치료제 지정’이 정점에 도달했던 것 또한 지난 2020년이어서 89건이 지정되었던 것으로 나타났다.
89건이라면 전년도의 30건에 비해 3배 가까이 껑충 뛰어오른 수치이다.
이는 바꿔 말하면 ‘소아 희귀질환 치료제 지정’ 프로그램이 제약업계가 소아 희귀질환 치료제들에 초점을 맞추도록 강화하는(reinforcing) 역할을 했음을 시사한다고 몰리 애널리스트는 풀이했다.
몰리 애널리스트는 “이처럼 괄목할 만한 결과가 지난 2014년 FDA가 소아 희귀질환 치료제들의 개발에 중점을 두기 시작하면서부터 나타난 성과물이라 할 수 있을 것”이라고 말했다.
‘소아 희귀질환 치료제 지정’ 프로그램의 도입으로 소아 희귀질환 치료제들의 허가건수가 증가하는 성과로 귀결되었다는 설명이다.
몰리 애널리스트는 “비록 ‘소아 희귀질환 치료제 지정’ 프로그램이 시장에 미친 직접적인 영향은 불명확하더라도 지난 2016년부터 ‘소아 희귀질환 치료제 지정’ 프로그램의 적용과 소아 희귀질환 치료제들의 허가건수가 동반상승한 것은 FDA가 금전적인 인센티브 부여를 지속해 신약개발을 위한 제약사들의 노력을 촉진시켜야 할 필요성을 시사하는 것”이라고 피력했다.
이에 따라 ‘소아 희귀질환 치료제 지정’ 프로그램이 폐지됨에 따라 미래의 소아 희귀질환 치료제 시장에 불확실성이 고조되기에 이른 만큼 새로운 정책적 노력이 강구되어야 할 것이라고 몰리 애널리스트는 결론지었다.
차후 소아 희귀질환 치료제들의 개발과 허가취득을 촉진시키기 위한 (‘소아 희귀질환 치료제 지정’ 프로그램의) 후속 프로그램이 도입되어야 할 것이라는 단언이다.
“소아는 작은 어른이 아니다”라는 소아의학계의 오랜 원칙을 새삼 상기케 하는 요즘이다.
-
01 차바이오그룹, 'CGB' 상량식 ...CGT 분야 단... -
02 코스피 제약바이오 1Q자기자본이익률 'SK바... -
03 "정부 육성지원 정책 뒷받침되면 제약바이오... -
04 동아참메드, 살균소독티슈 ‘이디와입스에이... -
05 아미코젠·퓨리오젠, 중국 정제시장 공략 ‘... -
06 큐라클,알츠하이머 신약 후보물질 ‘CU71’ PC... -
07 씨이랩-바이오써포트와 제약바이오 AI 품질... -
08 경희대 규제과학과, '의약품 유효성 평가' ... -
09 [약업 분석] 6월 신약·바이오 임상3상 12건…... -
10 건보공단, 담배소송 항소심 총력전…"과학적 ...











