뉴스
식약처 ‘묶음형 대안’, 공동생동 본 취지 살릴까
“규제 바꾸는 것 아닌 내부 심사 개선으로 품질 향상 도모”
박선혜 기자 │ loveloveslee@yakup.com


입력 2020-05-14 06:00 수정 2020.05.14 07:54
식약처가 제네릭 의약품의 품질 개선을 위해 내놓은 ‘묶음형 대안’에 대해 애초 목적한 1+3 공동생동의 본 취지를 잘 살릴 수 있을 것인가에 관심이 모이고 있다.
13일 식품의약품안전처(이의경 처장)는 ‘묶음형’ 허가관리 변경안을 공개하면서 ‘제네릭의약품 국제 경쟁력 제고’의 일환이라고 밝혔다.
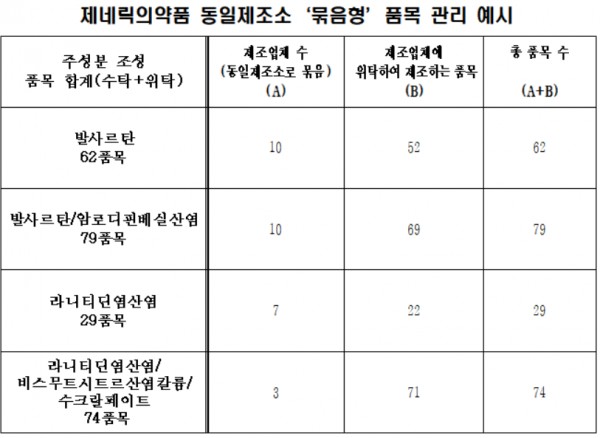
제네릭 '묶음형 허가'는 1개 제조소에서 제조되는 다수 업체의 제네릭은 제품명만 다를 뿐 제조소·원료·제조방법·생동자료 및 품질이 동일한 품목인 만큼, 일관성 있는 자료요건 등 허가·관리기준을 마련하고 이를 통일적으로 적용한다는 개념이다.
|
이는 제네릭 품질심사 절차를 개선하고 심사자료 검토 전담조직을 정비해 심사행정의 효율성과 일관성을 높여 우수한 품질의 제네릭의약품 유통환경을 조성하겠다는 취지에서 비롯됐다.
실상 묶음형 허가가 나타난 데는 지난달 24일 규제개혁위원회가 1+3 공동생동 안이었던 '의약품의 품목허가·신고·심사 규정 개정안'을 철회 권고한 배경이 있다.
당시 규개위의 입장은 공동생동 개정안이 2010년 규제개혁위원회가 폐지했던 규제와 유사할 뿐 아니라 제약업체의 시장진입 제한이 의약품 품질과 안전에 직접적인 개선 효과를 나타내지 못할 것이라는 판단이다.
이번 철회 결정으로 실상 식약처는 공동생동을 찬성했던 제약바이오협회와 더불어 대한약사회, 제약업계의 ‘모호하고 무책임한 정책 추진’이라는 비판을 피할 수 없었다.
이번 철회 결정으로 실상 식약처는 공동생동을 찬성했던 제약바이오협회와 더불어 대한약사회, 제약업계의 ‘모호하고 무책임한 정책 추진’이라는 비판을 피할 수 없었다.
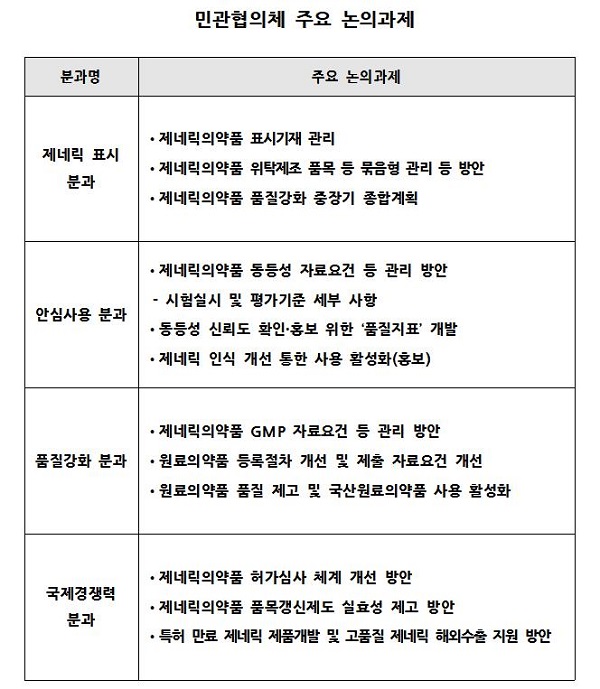
이후 식약처는 제네릭의약품 품질강화를 위한 또 다른 대안을 내놓기 위해 지난달 29일 민관협의체의 제약, 의사, 약사, 환자 등 4개 분과 대표와 모여 △제네릭 의약품 품질강화 종합계획, △묶음형 관리방안 △정확한 정보 제공방안 등을 논의했다.
|
이를 통해 결정된 것이 묶음형 관리방안인 것. 다만 관련 업계에서는 이번 조치가 공동생동의연장선이 아닌가에 대한 지적이 이어지고 있다.
식약처 관계자는 “공동생동 규제안의 연장선이라기보다 제네릭의 품질 향상을 위해 만든 내부적 절차라고 말할 수 있다”며 “정확히 어떤 차별성을 두고 있냐는 세부사항 등이 결정되면 설명할 수 있다”고 말했다.
무엇보다 식약처는 제네릭의 난립을 막고 전반적인 품질을 강화하고자 하는 ‘취지’를 강조했다. 새로운 대안으로 심사기간이 단축되고, 그동안 각 지방청별로 심사해 발생한 눈높이 차이가 상당 부분 해소되면서 불순물 검출 예방도 높이겠다는 목적이다.
식약처 관계자는 “이번 대안은 내부 심사 절차 개선안으로 규제에 영향을 주는 것은 아니다. 따라서 규개위의 결정이 필요한 것은 아니기 때문에 세부 사항이 정해지는 데로 시행될 것”이라고 밝혔다.
이어 “효율성 부분을 강조하고자 한다. 당장 허가를 신청한 업계 측에 변화가 오는 부분은 아니다. 이로 인한 허가신청 접수 및 처리기간 등 기타 변동은 없을 것”이라고 강조했다.
이어 “효율성 부분을 강조하고자 한다. 당장 허가를 신청한 업계 측에 변화가 오는 부분은 아니다. 이로 인한 허가신청 접수 및 처리기간 등 기타 변동은 없을 것”이라고 강조했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











