뉴스
옵디보·키트루다, PD-L1으로 묶인 가운데 ‘미묘한 차이’
옵디보 ‘적응증 확대’, 키트루다 ‘1, 2차 치료제로 모두 사용 가능’
전세미 기자 │ jeonsm@yakup.com


입력 2017-09-14 17:02 수정 2017.09.15 06:44
비소세포폐암 분야의 항 PD-L1 면역항암제 라이벌로 꼽히는 옵디보(성분명: 니볼루맙)와 키트루다(성분명: 펨브롤리주맙). 지난 8월 두 약제에 대한 급여 적용이 이뤄진 후 학계 및 언론을 대상으로 한 각 약제의 어필 포인트는 미묘하게 달랐다.
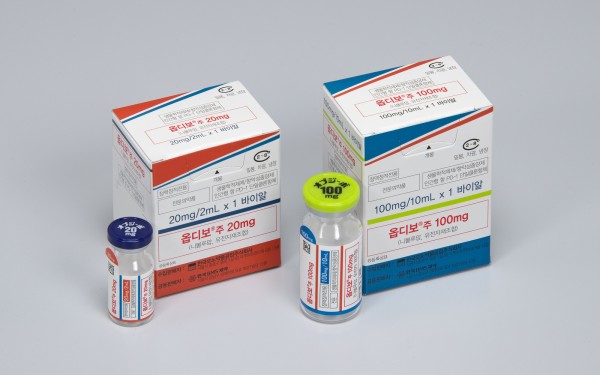
먼저 한국오노약품공업과 한국BMS제약의 ‘옵디보’는 기존의 적응증에 5개 적응증[신세포암, 방광암, 두경부암, 전형적 호지킨 림프종, 흑색종(옵디보+여보이 병용)]이 국내에서 추가 승인돼 총 7개 적응증을 보유하게 됐다. 이는 국내에서 허가된 면역항암제 중 가장 많은 적응증 개수다.
지난 13일 열린 옵디보 적응증 확대 기자간담회에서 강진형 교수(서울성모병원 종양내과)는 악성 흑색종에서의 옵디보와 여보이 병용요법 임상연구 CHECKMATE-067 결과와 적응증 확대의 의미를 발표했다.
이전에 치료 받은 적이 없는 BRAFV600E 변이 양성 또는 BRAF 야생형 진행성 악성 흑색종 환자를 대상으로 연구를 진행한 결과, 옵디보와 여보이 병용요법은 여보이 단독요법 대비 사망위험을 45% 감소시키며 유의미한 생존기간 개선을 보였다.
이어 신세포암, 방광암, 호지킨 림프종에서의 옵디보 임상시험 결과가 발표됐다. 신생혈관억제 치료를 받은 적이 있는 진행성 투명세포 신세포암 환자를 대상으로 연구를 진행한 CHECKMATE-025에서 2년간 추적 관찰한 결과, 옵디보는 에베로리무스 대비 1차 유효성 평가변수인 전체 생존기간을 유의하게 향상시킨 것으로 나타났다.
옵디보는 다양한 암종에서 PD-L1 발현 여부와 관계없이 적용 가능하다는 점을 최대 장점으로 내세우고 있다. 게다가 8월 21일부터는 이전 백금기반 화학요법에 실패한 국소 진행성 또는 전이성 비소세포폐암 환자 중 PD-L1 발현율이 10% 이상인 환자들을 대상으로 급여가 적용됐다.
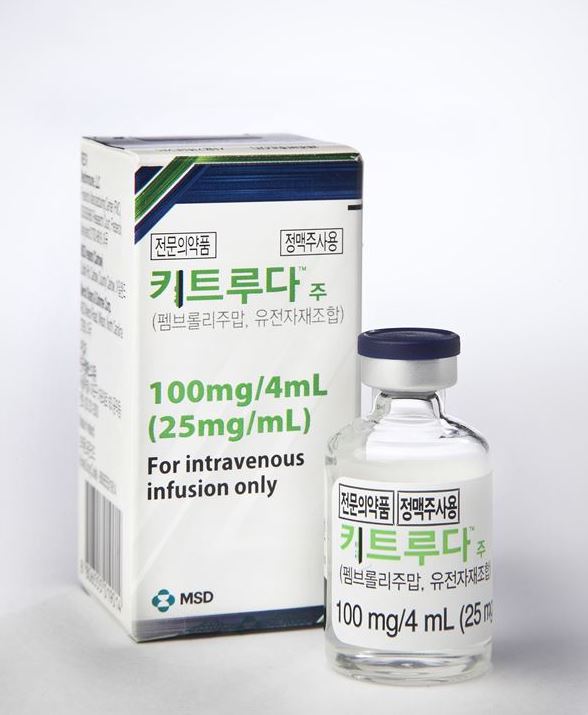
MSD의 ‘키트루다’도 급여가 적용됐지만, 옵디보와는 기준이 조금 다르다. 이전 백금기반 화학요법에 실패한 stage ⅢB 단계 이상의 환자에서 고식적 요법(palliative)을 2차 이상 진행한 상태여야 하고, PD-L1 발현율이 50% 이상이어야 한다.
보험 급여 적용의 바탕이 된 키트루다 임상 연구인 KEYNOTE-010은 진행성 비소세포폐암 환자 중 PD-L1 발현율이 1% 이상 발현하는 환자를 대상으로 진행한 임상시험이다. 연구 결과 PD-L1 발현율이 50% 이상인 환자에서 키트루다 투여군이 도세탁셀(Docetaxel) 투여군에 비해 전체 생존기간을 약 50% 개선시킨 것으로 나타났다.
급여 기준과 별개로 키트루다는 1차 치료에서도 사용할 수 있다는 것이 장점이다. 지난 3월 키트루다는 PD-L1 발현율 50% 이상인 환자에서 진행성 비소세포폐암 1차 치료제로 승인된 바 있다. 옵디보는 아직까지 1차 치료 적응증을 획득하지 못한 상태다.
그러나 PD-L1 발현율 50%를 바이오마커의 기준으로 삼는 것에 대해서는 그간 여러 시각차가 있었다. 면역항암제는 그 특성상 PD-L1 발현율 50% 이상의 환자들에 효과가 좋은 것으로 다수의 임상시험에서 밝혀진 바 있지만, PD-L1 발현율 50% 이하의 환자가 원한다면 비급여라도 사용을 허가해 주어야 한다는 일각의 주장들도 있었기 때문.
김봉석 교수(중앙보훈병원 혈액종양내과)는 “바이오마커로 인해 옵디보와 키트루다가 각각 처방할 수 있는 기준이 달라 접근성의 논란도 있겠지만, 두 약제 간 직접적인 비교가 이루어지지 않았기 때문에 선뜻 비교하기는 어렵다. 급여 이후 실제 현장에서 처방이 이뤄져 이에 대한 검증이 돼야 할 것”이라고 말했다.
|
지난 13일 열린 옵디보 적응증 확대 기자간담회에서 강진형 교수(서울성모병원 종양내과)는 악성 흑색종에서의 옵디보와 여보이 병용요법 임상연구 CHECKMATE-067 결과와 적응증 확대의 의미를 발표했다.
이전에 치료 받은 적이 없는 BRAFV600E 변이 양성 또는 BRAF 야생형 진행성 악성 흑색종 환자를 대상으로 연구를 진행한 결과, 옵디보와 여보이 병용요법은 여보이 단독요법 대비 사망위험을 45% 감소시키며 유의미한 생존기간 개선을 보였다.
이어 신세포암, 방광암, 호지킨 림프종에서의 옵디보 임상시험 결과가 발표됐다. 신생혈관억제 치료를 받은 적이 있는 진행성 투명세포 신세포암 환자를 대상으로 연구를 진행한 CHECKMATE-025에서 2년간 추적 관찰한 결과, 옵디보는 에베로리무스 대비 1차 유효성 평가변수인 전체 생존기간을 유의하게 향상시킨 것으로 나타났다.
옵디보는 다양한 암종에서 PD-L1 발현 여부와 관계없이 적용 가능하다는 점을 최대 장점으로 내세우고 있다. 게다가 8월 21일부터는 이전 백금기반 화학요법에 실패한 국소 진행성 또는 전이성 비소세포폐암 환자 중 PD-L1 발현율이 10% 이상인 환자들을 대상으로 급여가 적용됐다.
|
보험 급여 적용의 바탕이 된 키트루다 임상 연구인 KEYNOTE-010은 진행성 비소세포폐암 환자 중 PD-L1 발현율이 1% 이상 발현하는 환자를 대상으로 진행한 임상시험이다. 연구 결과 PD-L1 발현율이 50% 이상인 환자에서 키트루다 투여군이 도세탁셀(Docetaxel) 투여군에 비해 전체 생존기간을 약 50% 개선시킨 것으로 나타났다.
급여 기준과 별개로 키트루다는 1차 치료에서도 사용할 수 있다는 것이 장점이다. 지난 3월 키트루다는 PD-L1 발현율 50% 이상인 환자에서 진행성 비소세포폐암 1차 치료제로 승인된 바 있다. 옵디보는 아직까지 1차 치료 적응증을 획득하지 못한 상태다.
그러나 PD-L1 발현율 50%를 바이오마커의 기준으로 삼는 것에 대해서는 그간 여러 시각차가 있었다. 면역항암제는 그 특성상 PD-L1 발현율 50% 이상의 환자들에 효과가 좋은 것으로 다수의 임상시험에서 밝혀진 바 있지만, PD-L1 발현율 50% 이하의 환자가 원한다면 비급여라도 사용을 허가해 주어야 한다는 일각의 주장들도 있었기 때문.
김봉석 교수(중앙보훈병원 혈액종양내과)는 “바이오마커로 인해 옵디보와 키트루다가 각각 처방할 수 있는 기준이 달라 접근성의 논란도 있겠지만, 두 약제 간 직접적인 비교가 이루어지지 않았기 때문에 선뜻 비교하기는 어렵다. 급여 이후 실제 현장에서 처방이 이뤄져 이에 대한 검증이 돼야 할 것”이라고 말했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 세종파마텍, '액상 캡슐 충전기' 국산화로 ... -
02 상장 제약·바이오사 2025년 평균 매출… 코스... -
03 약포지·시럽병 '수급 흔들'…약사회 "가수요 ... -
04 “AI 시대에도 결국 사람” 씨엔알리서치가 짚... -
05 [2026 기대 신약 TOP 10] ③ 다발성 골수종 ... -
06 미국 CVS 파마시, 드럭스토어서 약국으로 전환? -
07 [인터뷰] '서보 프레스'로 K-뷰티 설비의 글... -
08 리가켐바이오,파이안바이오와 신약 연구개발... -
09 '자보 8주 제한' 강행 논란…"보험사 이익·환... -
10 바이오포아, 국내 기술 PRRS 생백신 멕시코 ...











