6월부터 급여 적용…폐동맥고혈압 치료 접근성 및 패러다임 변화 기대


|
폐동맥고혈압(PAH)은 심장에서 폐로 혈액을 운반하는 폐동맥 내의 혈압이 상승해 폐동맥이 두꺼워지고, 폐의 혈액 순환이 저하되는 질환으로, 전체 폐고혈압의 약 3%를 차지하는 1군 희귀난치성 질환이다. 적절한 치료가 이뤄지지 않을 경우 우심부전으로 발전하거나 심한 경우 사망에 이르는 원인이 될 수 있어 주의가 필요하다.
문제는 이처럼 중증 질환임에도 불구하고 치료 옵션이 제한적이라는 점이다. 특히 1차 치료에서 충분한 반응을 보이지 않은 환자들이 선택할 수 있는 대안이 부족해 임상현장에서 미충족 수요가 높은 분야다.
2025년 6월 요양급여 인정, 기존 치료 제한 환자의 치료 옵션 및 접근성 확대
바이엘 코리아의 아뎀파스(리오시구앗)는 2014년 6월, 식품의약품안전처로부터 두 가지 적응증에 대해 허가를 받았다.
첫째는 ▲수술이 불가능하거나 수술 후에도 증상이 지속 또는 재발하는 만성 혈전색전성 폐고혈압(CTEPH, WHO Group 4) 성인 환자에서의 운동능력 개선이며, 둘째는 ▲WHO 기능분류 2~3 단계에 해당하는 폐동맥고혈압(WHO Group 1) 성인 환자의 운동능력 개선이다.
허가 이후 아뎀파스는 2025년 6월 보건복지부 고시에 따라 건강보험 약제 급여 목록에 등재됐다. WHO 기능분류 2~3단계의 PAH 환자 중 기존 ERA 및/또는 PDE-5 억제제에 충분한 반응을 보이지 않거나 ERA 및 PDE-5 억제제 폐동맥고혈압 약제에 모두 금기인 경우 급여가 적용된다.
NO와 무관하게 sGC를 직접 자극하는 작용 기전

|
아뎀파스는 폐동맥고혈압 및 만성 혈전색전성 폐고혈압 치료에 허가된 최초의 가용성 구아닐산 고라화효소(sGC) 자극제이다. 일산화질소(NO)의 존재 여부에 상관없이 NO-sGC 작용경로 내에서 효과를 발휘하는 이중 작용 기전을 갖고 있다. NO가 존재할 경우 NO와 sGC의 결합을 안정화시켜 낮은 수준의 농도에서도 반응할 수 있도록 민감도를 증가시키며, NO가 존재하지 않더라도 다른 결합 부위를 활용해 sGC를 직접 자극해 혈관 확장에 필요한 cGMP 생성을 유도한다. 이러한 기전을 통해 혈관이 이완되고, 세포 증식과 섬유화가 억제되며, 폐혈관 저항이 감소함으로써 심혈관 기능을 개선하는 데 기여한다.
PDE-5 억제제 대신 아뎀파스 전환 투여시 유의한 임상적 개선 확인

|
REPLACE 연구에서는 기존 PDE-5 억제제 치료에 반응이 불충분한 증상적 폐동맥고혈압 환자들을 대상으로 아뎀파스로의 전환 투여가 치료 효과 향상에 기여할 수 있음을 확인했다. 24주 시점에서 임상적 악화 없이 임상적 개선 기준을 달성한 환자 비율은 아뎀파스 전환 투여군이 41%로 나타났으며, 이는 PDE-5 억제제 유지 투여군에 비해 2.78배 높은 수치다.
주요 평가 지표인 6분 보행거리 변화에서도 아뎀파스 전환군이 유지군보다 더 큰 개선 폭을 보였다. 주목할 점은 안전성 측면에서의 결과다. 임상적 악화 발생 사례는 아뎀파스 전환 투여군에서 1건(1%)에 불과했던 반면, PDE-5 억제제 유지 투여군에서는 10건(9%)으로 보고되어, 아뎀파스 전환 시의 임상적 악화 위험이 유지군 대비 90% 낮은 것으로 나타났다. 이상반응의 전체 빈도는 두 군 간 유사했으나, 중대한 이상반응은 PDE-5 억제제 유지군에서 더 많이 발생했다.
2년 이상의 장기 추적 연구로 임상적 효능과 장기 안전성 프로파일 확인
|
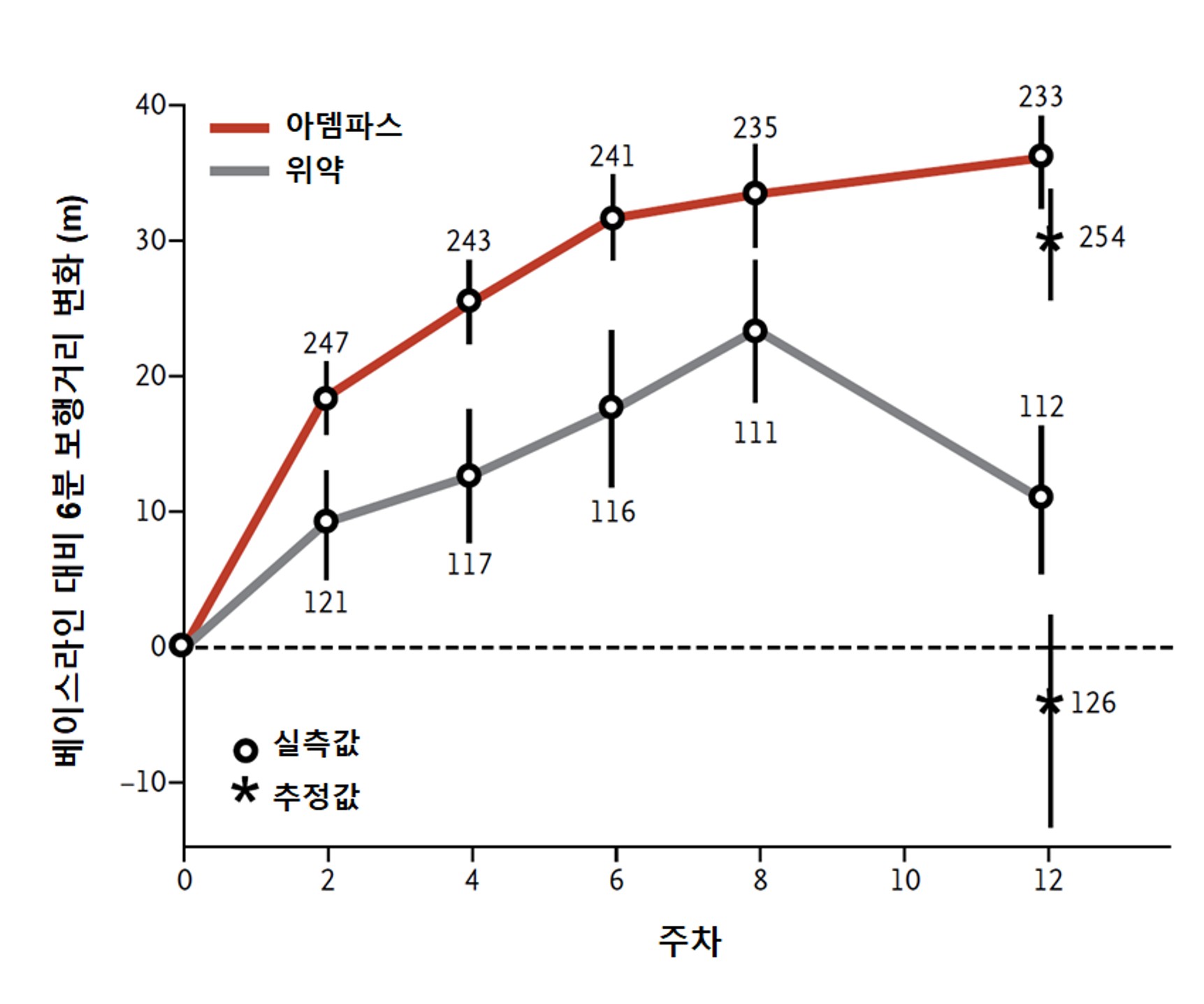
아뎀파스의 임상적 효능과 안전성 프로파일은 PATENT 연구를 통해서도 확인됐다. PATENT-1 연구에서는 아뎀파스 투여군이 위약군에 비해 6분 보행거리(6MWD)에서 유의미한 운동능력 개선을 보였다. 아뎀파스 투여군에서는 베이스라인 대비 30m 증가한 반면, 위약군은 6m 감소하여 두 치료군 간 총 36m의 차이를 보였다.
또한 아뎀파스 투여 시 폐혈관 저항, NT-proBNP 등 심혈관 지표에서도 긍정적인 변화가 확인되었으며, ERA 또는 프로스타노이드 병용 여부와 관계없이 치료 효과는 일관되게 나타났다. 특히 WHO 기능등급이 상대적은 높은, 즉 증상이 더 심한 환자군에서 아뎀파스의 치료적 이점이 더욱 뚜렷하게 나타났다.
장기 지속 투여에 대한 안전성과 효과는 PATENT-2 연구에서도 확인되었다. 2년간의 추적 관찰 결과, WHO 기능등급과 6분 보행거리 개선이 안정적으로 유지되었고 NT-proBNP 수치도 추적 기간동안 낮은 수준을 유지했다. 평가변수에 포함된 이러한 지표들은 전체 생존기간(OS)과도 유의한 상관관계를 보여, 아뎀파스의 장기적 치료 가치를 확인했다.
글로벌 가이드라인이 권고하는 아뎀파스 전환 치료 전략
전환 투여의 임상적 효과와 장기 안전성 프로파일을 확인한 임상 연구 결과를 바탕으로 sGC 자극제인 아뎀파스는 2022년 유럽심장학회(ESC)/유럽호흡기학회(ERS) 폐동맥고혈압 약물치료 가이드라인 알고리즘에서 권고되는 주요 치료제 중 하나로 이름을 올리고 있다. 심폐 동반질환을 보유하지 않은 환자가 PDE-5 억제제 및 ERA 기반 단독요법 또는 병용요법을 진행한 이후의 추적관찰에서 중등도-저위험 환자로 분류될 경우, PRA(프로스타글란딘 수용체 작용제) 추가(Class IIa) 또는 PDE-5 억제제에서 sGC로의 전환 투여(Class IIb)가 권고된다.
-
01 LG화학, 미국 프론티어-메디신즈 항암제 후... -
02 랩지노믹스,유투의료재단과 검체위수탁사업 ... -
03 삼성제약, '삼성로수바스타틴정20밀리그램' ... -
04 HK이노엔,아토피 피부염 치료제 임상1b상 I... -
05 아이빔테크놀로지,미국 CSHL·프랑스 IPAM 등... -
06 지오영 그룹, 창사 이래 첫 매출 5조 돌파 -
07 지투지바이오, SIRS서 3대 CNS 질환 타깃 '... -
08 일라이 릴리, 영국 센테사 파마 최대 78억달... -
09 '거점도매' 공방 확산…대웅, 공급망 투명성 ... -
10 "생존 전쟁" 선포…유통협회, 대웅 '거점도매...











