뉴스
베링거 미라펙스정 등 4품목 허가사항 변경
하지불안증후군 환자 예상치 못한 유해사례 1건 보고
이혜선 기자 │ lhs@yakup.com


입력 2012-11-30 06:06 수정 2012.11.30 07:21
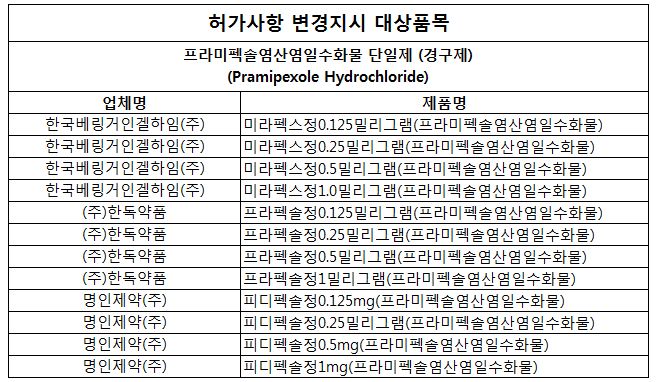
한국베링거인겔하임의 미라펙스 정 0.125mg 등 프라미펙솔염산염일수화물 4품목에 대한 허가사항이 변경돼 병의원 및 약국에서 변경 사항을 잘 숙지해야 한다.
식약청은 프라미펙솔 단일 경구제의 시판후 사용경험에서 예상하지 못한 유해사례로 장폐색증과 하지불안증후군 환자에서의 무력증 등이 각각 1건씩 보고된 것을 사용상 주의사항에 추가했다.
장폐색증은 기존에 새로운 이상반응에서 예상하지 못한 유해사례로 변경됐다. 하지불안증후군 환자에게서 시판 전 임상시험에서 나타나지 않았던 예상치 못한 유해사례로 무력증이 1건 보고됐다.
이번 주의사항 변경은 국내에서 재심사를 위해 4년 동안 651명을 대상으로 실시한 사용성적조사 결과, 인과관계에 상관없이 유해사례발현율은 1.54%(10/651명, 12건)로 보고됐다.
이 중 이 약과 인과관계를 배제할 수 없는 약물유해반응 발현율은 1.38%(9/651명, 11건)이다.
보고된 약물유해반응으로는 소화불량이 0.46%(3/651명, 3건)로 가장 많았고 그 다음은 구역이 0.31%(2/651명, 2건), 상복부불쾌감, 위식도역류, 구토, 부종, 무력증 및 환각이 각각 0.15%(1/651명, 1건)의 순으로 나타났다.
중대한 유해사례는 보고되지 않았지만 하지불안증후군 환자에서 시판 전 임상시험에서 나타나지 않았던 예상하지 못한 유해사례로 무력증이 1명에서 1건 보고됐다.
|
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 나노엔텍, 상반기 ‘ADAM-rWBC2’ 장비 수요 ... -
02 휴젤, 상반기 매출 2,000억 돌파…사상 최대 ... -
03 제이피아이헬스케어, 코스닥 도전…글로벌 영... -
04 휴온스, 2분기 영업이익 131억 원…전년比 40... -
05 '초읽기' 미국 의약품 관세 부과 ...예상 시... -
06 동국생명과학, MRI 조영제 생산설비 확대…핵... -
07 질병관리청- IVI, CEPI 세계 최대 백신 평가... -
08 LG생건 체취 케어 브랜드 ‘46cm', 레드닷 디... -
09 대웅제약, 산업안전보건 발표대회 2관왕… ‘... -
10 코스맥스, 극한환경 미생물 유래 항산화 효...











