뉴스
일반 의료기기와 같지만 다른 ‘체외진단의료기기’
일반 의료기기 규제 속 관리되지만 등급 분류 기준 등 미세하게 달라
전세미 기자 │ jeonsm@yakup.com


입력 2017-07-13 06:00 수정 2017.07.13 06:00
혈액검사 시약, 임신 테스트기, 자가 혈당 측정을 위한 일회용 스트립(strip). 이들의 공통점은 무엇일까? 바로 ‘체외진단의료기기’이다.
최근 많은 의료기기들이 첨단화 됨에 따라 일반 의료기기 뿐 아니라 체외진단의료기기에 대한 관심 또한 증가하는 추세다.
지난 11일 고대구로병원 의생명연구센터에서는 ‘제9회 In Vitro Diagnostic Medical Device International Symposium’이 개최돼 각계 전문가들이 최신 지견을 나누는 시간을 가졌다.

|
우 주무관은 “이를 일원화하기 위해 2010년 식약처에서는 TF Team을 만들어 본격적인 관리에 나섰다. 그 결과 2014년 기존의 진단용 시약 및 체외진단의약품까지도 의료기기로 관리하는 것으로 변경됐다”고 말했다.
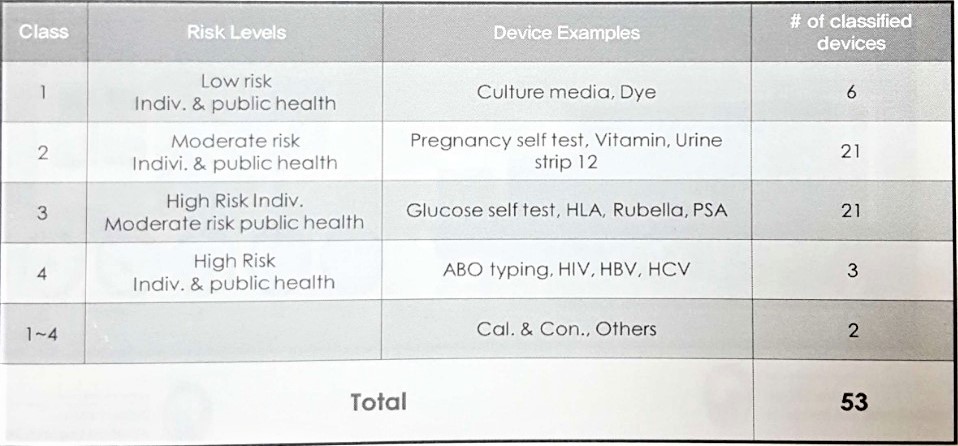
우 주무관은 “일반 의료기기는 4등급 분류체계다. 이 체계는 잠재적인 위험성에 따라 분류되며 4등급으로 갈수록 위험도가 높다는 것을 뜻한다. 이 중 가장 많은 기기가 해당하는 등급이 2등급이다”라고 설명했다.
이어 우 주무관은 “체외진단의료기기도 4등급으로 분류돼있지만, 일반 의료기기와 등급 분류를 나누는 기준이 다르다. 체외진단의료기기는 개인·공중의 위해도가 굉장히 중요하다. 예를 들어 메르스나 지카 바이러스와 같은 전염성을 띈 질병에 체외진단의료기기가 사용될 경우는 개인 및 공중의 위해도가 높다”고 말했다.
현재 허가된 체외진단의료기기는 총 53 품목이며, 대표적으로 혈액학 검사를 위한 시약, 소변 및 대변의 화학 농도 측정을 위한 시약, 자가 혈당 측정을 위한 스트립, 임신 테스트기 등이 있다.
|
우 주무관은 “일반 의료기기 승인을 위해서는 기술문서 심사 자료와 성능시험 자료가 필요하다. 그러나 체외진단의료기기는 취급자의 안전이 매우 중요하기 때문에 인증 신청 시 취급자 안전에 대한 자료를 별도로 제출해야 한다”고 설명했다.
우 주무관은 “일반 의료기기는 법과 시행령, 시행 규칙 등 식약처장이 세부규칙을 고시하는 것으로 이뤄진다. 그러나 체외진단의료기기는 의료기기법 안에서 다뤄지고 있다. 이에 최근 체외진단의료기기 관련법을 제정하기 위해 다방면으로 노력하고 있다”고 설명했다.
이어 그는 “체외진단의료기기 분야는 앞으로 발전이 무한한 분야 중 하나다. 이에 따른 업계의 관심이 높은 만큼 식약처 역시 체외진단의료기기의 발전을 위해 노력할 것”이라고 덧붙였다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 미래의료혁신연구회,제약산업 구조 전환-글... -
02 차바이오텍,밀테니바이오텍과 차세대 항암 ... -
03 아미코젠, 농식품부 ‘국가 바이오소부장 국... -
04 일본 이세(ISE) 홀딩스, “한국 홍삼란 기술 ... -
05 아리바이오,경구 알츠하이머 치료제 임상3... -
06 지엔티파마,중국 휘유와 뇌졸중 치료제 '넬... -
07 설덕인 원장, “천연물 기반 질염 치료제 개... -
08 에이비엘바이오-컴퍼스, 담도암 2차 ‘토베시... -
09 "치매 극복, 내게 맡겨라" 뉴로핏·큐어버스·... -
10 인게니움테라퓨틱스, 중국 '리피오르 바이오...










