뉴스
차세대 바이오의약품 R&D 10년 새 기하급수, CAR-T·mRNA 성공 열풍 불지펴
파이프라인 960개, 42% 항종양 타깃…초기 개발단계 대다수
권혁진 기자 │ hjkwon@yakup.com


입력 2023-03-10 06:00 수정 2023.03.10 06:01
최근 10년 새 차세대 바이오치료제 연구개발 활동이 기하급수로 증가했다. CAR-T, mRNA 백신 성공사례에 힘입어 향후 바이오치료제 열풍은 지속될 전망이다.
아이큐비아 휴먼 데이터 사이언스팀(IQVIA Institute for Human Data Science)은 지난 3일 '전 세계 R&D 트렌드 2022(Global Trends in R&D 2022)' 보고서를 발간했다. 보고서엔 최근 신약개발 연구개발 동향이 담겼다.
연구팀은 2012년부터 2022년까지 전 세계 차세대 바이오 신약개발 파이프라인이 1000개에 육박할 만큼 급성장했다고 전했다. 연구팀은 특히 유전자·세포치료제 연구가 비교적 최근에 시작됐음에도 블록버스터가 탄생했고, 해당 분야 후보물질이 가파르게 증가하는 만큼 향후 긍정적인 결과가 기대된다고 덧붙였다.
차세대 바이오치료제에는 세포치료제, 유전자치료제 및 백신, 세포·유전자치료제, 유전자 편집 기반 치료제 등이 포함된다.
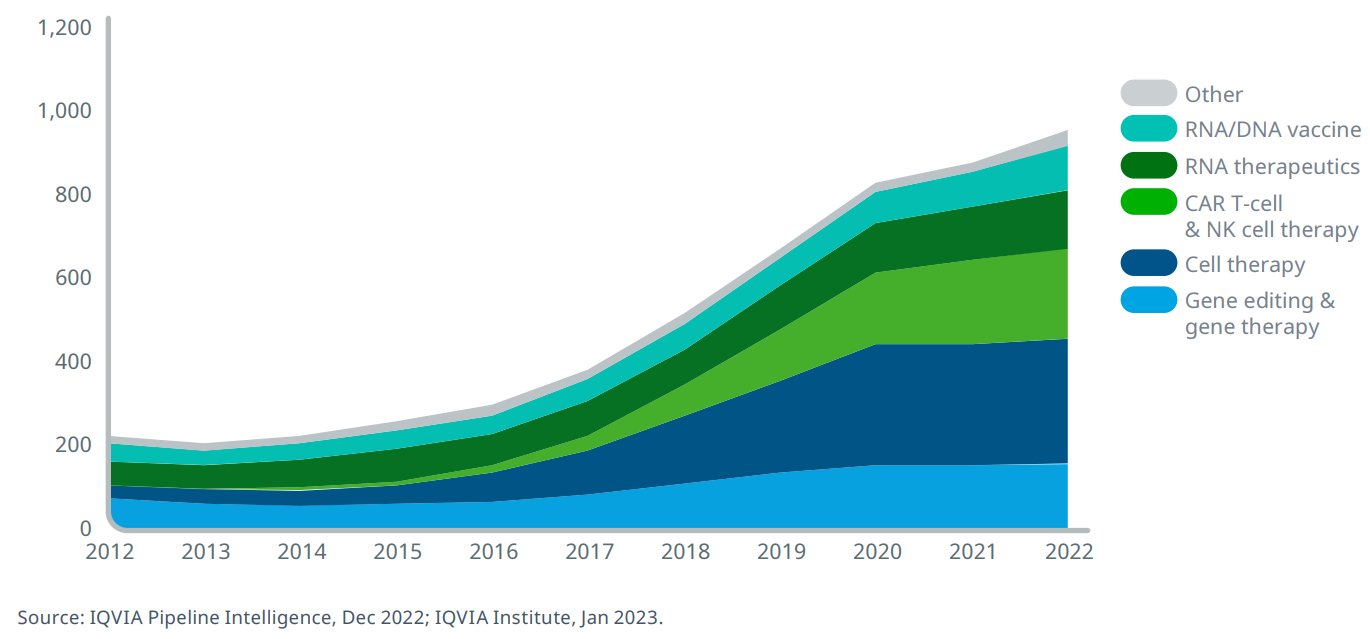
△2012년부터 2022년까지 작용 매커니즘 별 임상 1상부터 규제 승인 단계에 있는 차세대 바이오치료제 개수(Next-generation biotherapeutics Phase I to regulatory submission pipeline by mechanism, 2012–2022).
지난 2012년부터 2022년까지 전 세계 임상 1상부터 BLA 단계(승인을 위한 인허가)에 있는 차세대 바이오치료제 파이프라인은 총 960개로 집계됐다. 차세대 바이오치료제 임상개발은 2017년부터 연평균성장률 20%로 급성장하고 있다.
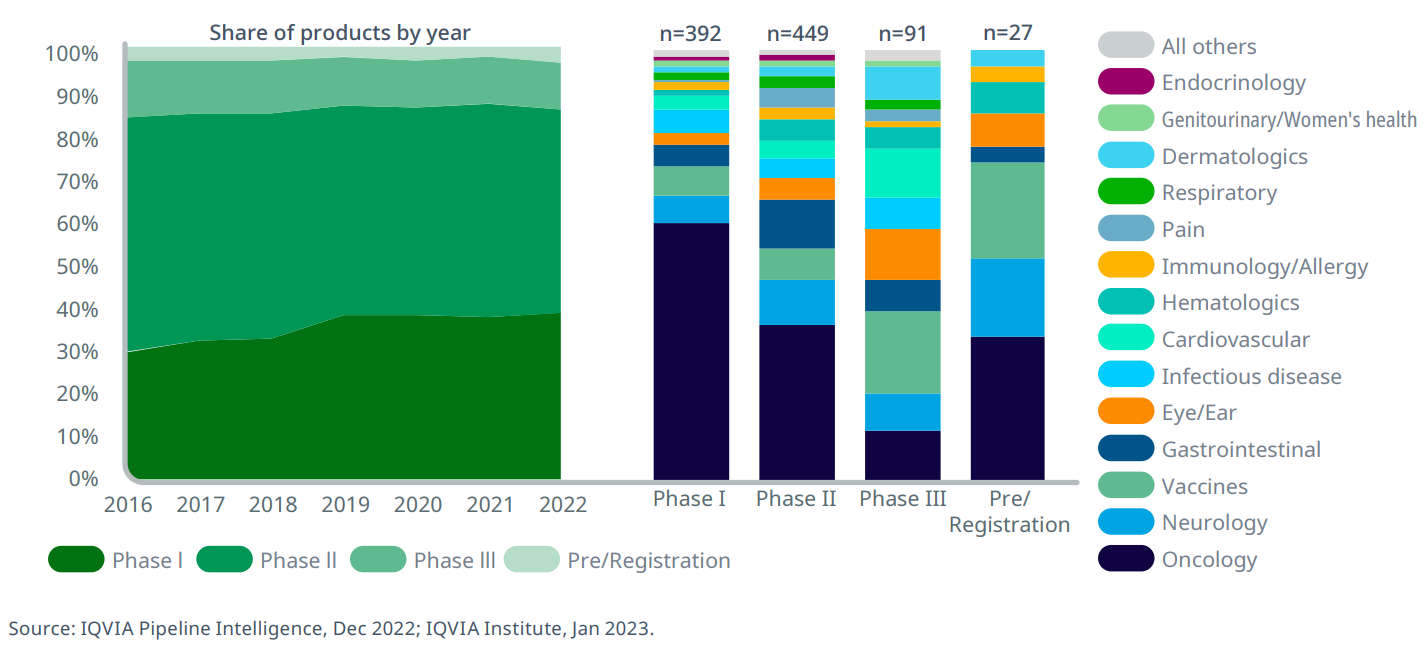
차세대 바이오치료제 파이프라인 중 42%는 항종양을 타깃하는 것으로 분석됐고, 전체 파이프라인 중 약 85%는 임상 1상과 2상 단계에 있는 것으로 나타났다. 임상 1상 단계에는 파이프라인이 392개가 집계됐고, 임상 2상 449개, 임상 3상 91개로 나타났다. 승인을 위한 인허가 단계에는 27개의 파이프라인이 있는 것으로 나타났다.
임상 1상 단계에는 항종양 타깃 파이프라인이 가장 많았고, 신경계 질환, 백신이 뒤를 이었다. 반면 임상 3상 단계에는 백신이 신경계 파이프라인보다 전체 중 큰 비중을 차지했다.
또한 차세대 바이오치료제 파이프라인 중에는 세포치료제가 가장 큰 비중을 차지하는 것으로 나타났다. 세포치료제 파이프라인 중 40%는 다양한 암종과 희귀하지 않은 고형암을 타깃했다.
특히 CAR-T 세포치료제와 NK 세포치료제는 2012년 이전까지 데이터에 집계되지 않았으나, 2012년부터 2022년까지 총 217개의 파이프라인이 주요 임상 및 인허가 단계에 있는 것으로 분석됐다.
CRISPR-Cas9과 같은 유전자 편집 기술 기반의 유전자치료제는 2010년 이후 지속적인 성장세를 나타내고 있다. 이 연구개발 분야에는 위장질환이 26%로 가장 많았고, 이어 눈·귀 질환 타깃이 16%를 차지했다. 비교적 최근 등장한 RNA 기반 치료제는 차세대 바이오치료제 파이프라인에서 차지하는 비중이 미미했다.
연구팀은 “차세대 바이오치료제가 임상시험 후반 단계와 인허가 단계에서 극히 적은 것은 신약개발 특성도 있지만, 그만큼 차세대 바이오치료제 개발이 어렵다는 것을 의미한다”고 전했다.
이어 “최근 CAR-T 세포치료제 성공과 코로나19 백신 개발을 위한 mRNA 및 DNA 백신 기술 개발의 발전은 차세대 백신 연구개발 활동에 상당한 증가를 가져왔다”라며 “최근 핵산 기반 차세대 백신이 다른 질병에 적용되는 것은 주목할만하다”고 덧붙였다.
아이큐비아 휴먼 데이터 사이언스팀(IQVIA Institute for Human Data Science)은 지난 3일 '전 세계 R&D 트렌드 2022(Global Trends in R&D 2022)' 보고서를 발간했다. 보고서엔 최근 신약개발 연구개발 동향이 담겼다.
연구팀은 2012년부터 2022년까지 전 세계 차세대 바이오 신약개발 파이프라인이 1000개에 육박할 만큼 급성장했다고 전했다. 연구팀은 특히 유전자·세포치료제 연구가 비교적 최근에 시작됐음에도 블록버스터가 탄생했고, 해당 분야 후보물질이 가파르게 증가하는 만큼 향후 긍정적인 결과가 기대된다고 덧붙였다.
차세대 바이오치료제에는 세포치료제, 유전자치료제 및 백신, 세포·유전자치료제, 유전자 편집 기반 치료제 등이 포함된다.
|
지난 2012년부터 2022년까지 전 세계 임상 1상부터 BLA 단계(승인을 위한 인허가)에 있는 차세대 바이오치료제 파이프라인은 총 960개로 집계됐다. 차세대 바이오치료제 임상개발은 2017년부터 연평균성장률 20%로 급성장하고 있다.
차세대 바이오치료제 파이프라인 중 42%는 항종양을 타깃하는 것으로 분석됐고, 전체 파이프라인 중 약 85%는 임상 1상과 2상 단계에 있는 것으로 나타났다. 임상 1상 단계에는 파이프라인이 392개가 집계됐고, 임상 2상 449개, 임상 3상 91개로 나타났다. 승인을 위한 인허가 단계에는 27개의 파이프라인이 있는 것으로 나타났다.
|
△2012년부터 2022년까지 타깃 질환별 임상 1상부터 규제 승인단계에 있는 차세대 바이오치료제 개수(Next-generation biotherapeutic products pipeline by phase and therapeutic drug clas).
임상 1상 단계에는 항종양 타깃 파이프라인이 가장 많았고, 신경계 질환, 백신이 뒤를 이었다. 반면 임상 3상 단계에는 백신이 신경계 파이프라인보다 전체 중 큰 비중을 차지했다.
또한 차세대 바이오치료제 파이프라인 중에는 세포치료제가 가장 큰 비중을 차지하는 것으로 나타났다. 세포치료제 파이프라인 중 40%는 다양한 암종과 희귀하지 않은 고형암을 타깃했다.
특히 CAR-T 세포치료제와 NK 세포치료제는 2012년 이전까지 데이터에 집계되지 않았으나, 2012년부터 2022년까지 총 217개의 파이프라인이 주요 임상 및 인허가 단계에 있는 것으로 분석됐다.
CRISPR-Cas9과 같은 유전자 편집 기술 기반의 유전자치료제는 2010년 이후 지속적인 성장세를 나타내고 있다. 이 연구개발 분야에는 위장질환이 26%로 가장 많았고, 이어 눈·귀 질환 타깃이 16%를 차지했다. 비교적 최근 등장한 RNA 기반 치료제는 차세대 바이오치료제 파이프라인에서 차지하는 비중이 미미했다.
연구팀은 “차세대 바이오치료제가 임상시험 후반 단계와 인허가 단계에서 극히 적은 것은 신약개발 특성도 있지만, 그만큼 차세대 바이오치료제 개발이 어렵다는 것을 의미한다”고 전했다.
이어 “최근 CAR-T 세포치료제 성공과 코로나19 백신 개발을 위한 mRNA 및 DNA 백신 기술 개발의 발전은 차세대 백신 연구개발 활동에 상당한 증가를 가져왔다”라며 “최근 핵산 기반 차세대 백신이 다른 질병에 적용되는 것은 주목할만하다”고 덧붙였다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 한국콜마, 세계적 화학기업 '바스프' 손잡... -
02 '2000억원' 규모 26년 국가신약개발사업 스... -
03 대한약사회, 건보공단 특사경 도입 '찬성'…... -
04 대한약사회, 대웅제약에 '블록형 거점도매 ... -
05 한올바이오, 오송 특화공장 신축 투자 중단 -
06 한국유니온제약,M&A 공고...'스토킹호스' 방... -
07 IVI-질병관리청, 팬데믹 대응 임상시험검체... -
08 GC녹십자, 코로나19 mRNA 백신 국내 임상 1... -
09 마이크로디지탈, 셀트리온 생산공정에 ‘더... -
10 디앤디파마텍, “FDA의 AI 기반 MASH 조직 분...











