뉴스
국내개발 의약품 11품목 미국·EU 인허가 장벽 뜷었다
삼성바이오에피스 5품목 '최다', 11품목중 8품목이 '바이오시밀러'
김용주 기자 │ yjkim@yakup.com


입력 2018-03-07 06:20 수정 2018.03.07 09:09
|
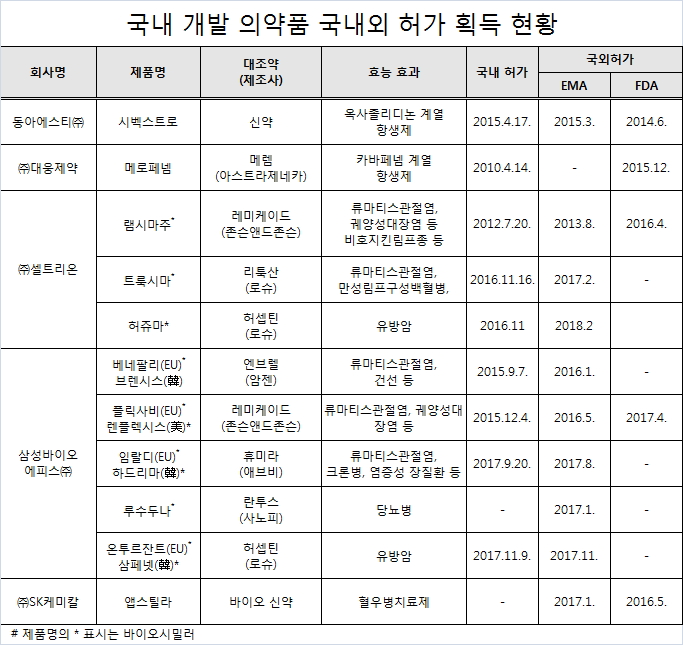
지난 2013년 이후 국내 제약사들이 개발한 의약품 11개가 미국과 EU의 인허가 장벽을 뚫고 판매가 본격화된 것으로 나타났다.
보건복지부에 따르면 지난 2013년 8월 셀트리온의 램시마주가 유럽의약품청(European Medicines Agency, EMA)의 허가를 받은 것을 시작으로 2017년 11월 삼성바이오에피스의 '온투르잔트' , 2018년 2월 셀트리온의 '허쥬마'' 등 국내개발 의약품 11품목이 미국과 EU의 인허가 획득하고 선진국 시장에서 판매가 되고 있는 것으로 집계됐다.
회사별로는 삼성바이오에피스가 베네팔리·플릭사비·임랄디·루수두나·온투르잔트 등 5품목으로 가장 많았고, 셀트리온이 램시마주·트룩시마·허쥬마 등 3품목이었다.
동아에스티 '시벡스트로', 대웅제약 '메로페넴', SK케미칼 '앱스틸라'도 미국과 유럽에서 인허가를 획득했다.
미국과 유럽에서 인허가를 획득한 11품목중 동아에스티 '시벡스트로', 대웅제약 '메로페넴' SK케미칼 '앱스틸라' 등 3품목을 제외한 나머지 8품목은 바이오시밀러였다. 이는 자체 개발한 신약보다 바이오시밀러가 글로벌 경쟁력이 높다는 것을 의미하는 것이다.
또 동아에스티의 '시벡스트로'. 셀트리온의 '램시마주', 삼성바이오에피스의 '플릭사비', SK케미칼의 '엡스틸라' 등 미국 FDA와 EU EMA의 허가를 받은 품목으로 조사됐다.
[관련기사]
미국 의약품시장은 '난공불락?'...제약바이오기업 진출 가속
2017-08-07 06:30
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 셀트리온, 현장 중심 직판 성과...주요 제품... -
02 이수그룹, 출범 30주년 ..배터리•AI•바이오 ... -
03 케이바이오솔루션, 휴덴스바이오 골이식재 ... -
04 엑셀세라퓨틱스, 국산 원부자재 제조 지원사... -
05 차백신연구소,대상포진 백신 2상 첫 환자 등... -
06 제놀루션, 꿀벌 낭충봉아부패병 동물용의약... -
07 콜마비엔에이치, 윤여원 대표이사 사임 -
08 이뮨온시아, 론자와 CDMO 계약…PD-L1 항체 ... -
09 세계 제약 · 바이오 · 건강기능 산업의 장 ‘... -
10 화이자 출신 약사, 팔로워 15만과 만든 세럼...











