뉴스
'사용량-약가 연동협상’ 환급제 적용대상 확대
보건복지부, 제약협회 통해 공지…약평위 인정 세포치료제 등 추가
최재경 기자 │ cjk0304@yakup.com


입력 2017-02-10 12:20 수정 2017.02.10 16:29
효율적인 약품비 관리를 위한 ‘사용량-약가 연동협상’ 환급제 적용 대상이 2월 1일부터 확대 된다. 보건복지부는 이 같은 내용을 담은 공문을 발송, 제약협회는 이를 10일 공지했다.
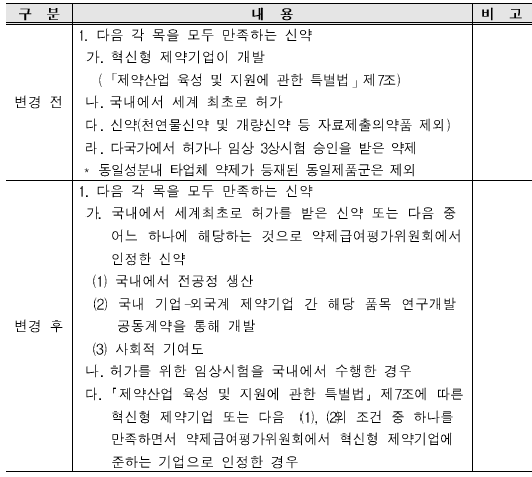
변경 전 '사용량-약가 연동협상’ 환급제 적용 대상은 △혁신형 제약기업이 개발한 신약 △국내에서 세계 최초로 허가받은 신약 △신약(천연물 신약 및 개량 신약 등 자료제출의약품 제외) △타국가에서 허가나 임상 3상 시험 승인을 받은 약제(*동일성분내 타업체 약제가 등재된 동일 재품군은 제외) 등 이었다.
변경 후인 2월부터는 △국내에서 세계최초로 허가를 받은 신약 또는 다음 증 어느 하나에 해당하는것으로 약제급여평가위원회(이하 약평위)에서 인정한 신약이 적용대상이 된다.
|

|
이는 국내에서 전공정 생산하거나, 국내 기업- 외국계 제약기업 간 해당 품목 연구개발 공동 계약을 통해 개발 된 품목이다.
또 △허가를 위한 임상시험을 국내에서 수행한 경우와 △제약산업 육성법에 따른 혁신형 제약기업 또는 약평위에서 혁신형 제약기업에 준하는 기업으로 인정한 경우 등이다.
이는 연 의약품 매출액 중 R&D 투자비율이 혁신형 제약기업의 평균 이상인 기업이나, 국내기업- 외국계 제약기업 간 개방형 혁신에 기반한 연구개발 투자 및 성과 창출 기업 등이다.
△약평위가 보건의료에 미치는 영향을 인정하는 세포치료제도 '사용량-약가 연동협상’ 환급제 적용대상에 포함된다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 삼성바이오로직스 파업 2일차…일부 공정 중... -
02 삼성바이오로직스 "교섭 지속했지만 합의 실... -
03 "K-제약바이오, 왜 아직 ‘블록버스터 신약’ ... -
04 "오가노이드 글로벌 생태계, 한국에 모인다"... -
05 파인트리테라퓨틱스, 아스트라제네카와 EGFR... -
06 셀트리온, 유럽 EMA에 ‘허쥬마SC’ 제형 추가... -
07 K-오가노이드 컨소시엄, 2026년 정기총회 개... -
08 한미사이언스, 1분기 경영 실적 발표… 전년... -
09 에스티젠바이오, ‘비티젠’으로 사명 변경… ... -
10 한미약품, 1분기 매출 3929억 달성… 원외처...










