
|
향정신성의약품인 '프로포폴' 등 23개 품목이 중점관리품목 마약류로 지정돼 관리가 강화된다. 또 오는 5월 18일부터 의료용 마약류 취급자는 마약류 취급내역을 '마약류통합관리시스템'을 통해 보고해햐 한다.
식품의약품안전처는 제약사, 도매상, 병‧의원, 약국 등 마약류취급자가 5월 18일부터 ‘마약류통합관리시스템’을 통해 마약류의약품 취급내역을 의무적으로 보고하는 것을 주요 내용으로 하는 '마약류 관리에 관한 법률 시행규칙'을 개정‧공포했다고 9일 밝혔다.
마약류통합관리시스템은 제조‧수입‧유통‧사용 등 마약류의약품 취급에 대한 모든 과정을 전산시스템으로 보고‧저장‧상시 모니터링하는 체계이다.
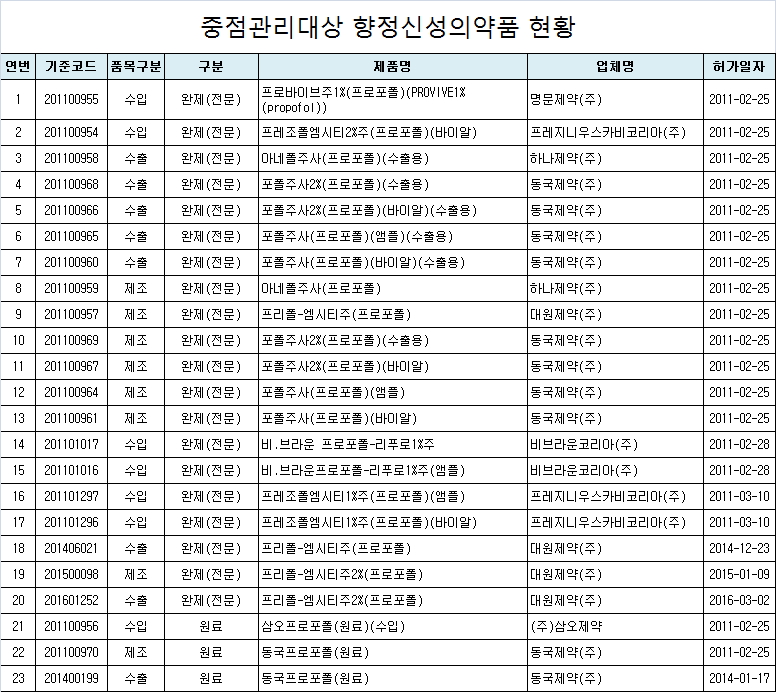
개정된 시행규칙에 따르면 사회적으로 오남용이 심각하거나 불법 유출되는 사례가 많았던 향정신성성의약품 ‘프로포폴’ 23품목을 '중점관리품목' 마약류로 신규 지정‧공고했다.
중점관리품목은 마약, 사회적으로 오남용이 심각하거나 불법 유출되는 사례가 많았던 향정신성의약품 등 식약처장이 지정‧공고한 향정신성의약품이다. 일반관리품목은 ‘중점관리품목’ 외 향정신성의약품, 동물용마약류 등이다.
개정안의 주요 내용은 △‘마약류통합관리시스템’을 통한 취급보고 의무화 일괄 시행 △마약류의약품을 ‘중점관리품목’과 ‘일반관리품목’으로 구분‧관리 △품목별로 마약류의약품 취급내역 보고 시점 합리적 조정 등이다.
마약류취급자는 2018년 5월부터 ’마약류통합관리시스템‘을 통해 모든 마약류의약품(마약, 향정신성의약품, 동물용 마약류 등)의 제조‧수입‧유통‧사용 등 취급 전 과정을 보고해야 한다.
마약류의약품을 ‘일련번호’ 정보를 기반으로 세부 취급내역까지 추적하는 ‘중점관리품목’과 ‘수량’ 정보를 중심으로 관리하는 ‘일반관리품목’으로 구분‧관리한다.
‘중점관리품목’의 경우 취급한 날로부터 7일 이내에 전산시스템으로 취급내역을 보고해야 하며, ‘일반관리품목’의 경우 취급한 달의 다음달 10일까지 전산시스템으로 보고해야 한다.
다만 병‧의원과 약국의 경우 일반관리품목의 보고 항목 중 ‘제조번호’와 ‘유효기간’의 보고는 2년 동안 시행을 유예하기로 했다.
식약처는 이번 개정을 통해 마약류의약품의 투명한 관리와 더불어 투약‧조제 등이 이루어지는 의료현장에서 마약류 취급보고 효율성이 높아질 수 있을 것이라고 밝혔다.
아울러, 마약류취급자들이 시스템 사용에 불편을 겪지 않도록 매뉴얼 배포, 교육‧홍보, ‘마약류통합관리시스템’과 상용 프로그램 간 연계 등을 안내할 계획이다.
-
01 “기증 인체조직 미용 사용 금지해야”…국회서... -
02 한미약품,GLP-1 비만신약 '에페' 우여곡절 ... -
03 대웅제약, 항궤양제 '펙수클루' 인도네시아 ... -
04 동아에스티, '스티렌큐정' 급만성 위염 적응... -
05 셀루메드, 이상인 경영지배인 선임 -
06 진스크립트, 리브랜딩으로 과학·기술 위에 ‘... -
07 “보이지 않는 품질까지 검증”…자비스, X-ray... -
08 다이이산쿄, OTC 사업 매각…항암 중심 전환 -
09 릴리, '파운다요' 안전성 논란 반격…임상 통... -
10 [DIA 2026] AI로 임상 모니터링 혁신…메디데...











