뉴스
'면역세포+표준치료 병용' 교모세포종 치료 해법 제시
삼성서울병원 남도현 교수팀 규명…4~5년 내 임상 활용 기대
이승덕 기자 │ duck4775@yakup.com


입력 2017-07-11 13:09 수정 2017.07.11 13:05
국내 연구진이 종양의 빅데이터 분석을 통해 종양주변 미세환경의 면역세포가 교모세포종 항암 치료 내성에 관련돼 있음을 밝혔다.
이는 기존 치료와 면역 미세환경 조절을 통한 면역치료의 병용을 통한 뇌종양 치료의 방향을 제시하는 것으로 4~5년 내 임상 활용을 기대할 수 있다는 설명이다.

|
그 결과는 암 분야 세계 최고 학술지인 '캔서셀 (Cancer Cell, 영향력 지수 IF 27. 407)' 인터넷판에 7월 10일자로 우선 게재됐다. 이번 연구는 복지부 및 한국보건산업진흥원(선도형 특성화연구사업)의 지원을 받아 수행됐다.
교모세포종(Glioblastoma)은 뇌종양 중 가장 악성도가 높은 암으로 방사선 및 항암제 치료에도 불구하고 진단 후 기대 생존기간이 1년여에 불과한 난치성 암이다.
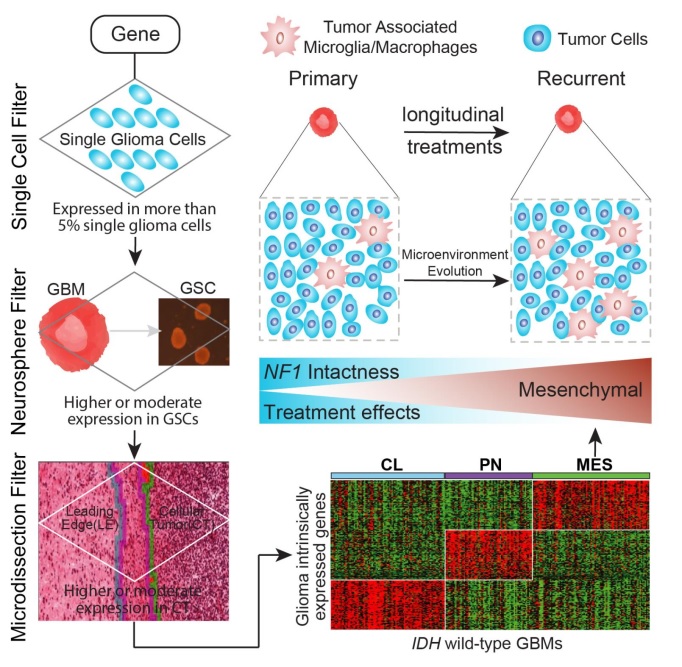
이번 연구에서는 교모세포종의 암조직, 환자유래세포, 종양 단일세포의 유전체 정보를 비교 분석해 종양 세포와 주변 미세환경 간의 상관관계를 분석했다.
분석 결과, 종양이 방사선 및 항암제 치료 후 항암내성을 획득해 진화하는 과정에 종양 주변의 면역세포가 관여됨을 밝혔다.
특히 종양이 진화하는 과정에서 종양주변 미세환경의 면역세포 중 M2대식세포(M2 macrophage)의 발현이 많아질수록 방사선 치료에 저항성이 높아지고, CD8+ T세포의 발현이 많아질수록 항암제 치료에 의한 과(過)돌연변이가 유도돼 항암제 치료에 대한 내성이 발생함에 따라 환자의 예후가 좋지 않음을 관찰했다.
이는 면역세포 발현을 억제함으로써 항암내성 발현을 억제할 수 있음을 나타내며, 기존의 표준 치료법과 면역 미세환경을 조절하는 면역 치료의 병용(倂用) 요법이 뇌종양 치료에 효과적일 수 있음을 제시한 것이다.
남도현 교수는 "이번 연구는 뇌종양 재발암 환자의 맞춤치료법 개발을 위한 기초자료로 향후 4~5년 이내에 임상에 활용될 수 있을 것으로 기대된다"며 "이를 위해 국제 공동연구 및 연구협력을 통한 빅데이터 구축 및 실용화를 위한 플랫폼의 고도화가 필요하다"고 제언했다.
2015년 남도현 교수팀은 뇌종양의 재발시 위치에 따른 시간적 유전체 진화 패턴의 규명해 빅데이터 분석과 항암내성 연구 방법을 국제 학계에 제시했다. (Cancer Cell, IF 27.407)
이어 2016년 한국, 미국, 일본, 이탈리아 임상-기초 연구자들과의 글로벌 유전체 공동연구를 통해 항암치료 후 종양 진화의 양상을 규명하고, 항암내성에 관여하는 유전자 표적을 제시했다.(Nature Genetics, IF 27.959)
올해 초에는 뇌종양 유전체의 다양성과 진화를 기반으로 하는 정밀의료 기술을 제시해 글로벌 리더십을 인정받은 바 있다. (Nature Genetics, IF 27.959)
|
남도현 교수는 "매번 실패하기만 하는 뇌종양 치료와의 승부에 도전하기 위해 암중개연구를 시작하게 됐다"며, "복지부에서 지원하는 난치암연구사업단에 선정돼 신개념의 치료를 현실화시킬 수 있는 인프라를 구축하고, 활발한 연구를 수행할 수 있었다"고 회고했다.
이어 "이번 연구를 통해 기존의 종양 진화와 관련한 유전체 기반 표적치료에 면역 미세환경 조절 치료제를 병용할 수 있는 과학적 근거를 제시함으로써 난치 질환인 뇌종양 치료 성공률을 높일 수 있을 것"이라고 기대했다.
복지부 김국일 보건의료기술개발과장은 "최근 남도현 교수 연구팀 보여준 우수한 성과들은 국제공동연구의 모범적인 사례로서, 국내 연구진의 글로벌 리더십 이 세계적인 성과로 이어질 수 있도록 연구 개발(R&D) 지원에 힘쓰겠다"고 밝혔다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 FDA, 중증 정신질환 치료제 개발 전폭 지원한다 -
02 메지온, FDA 공식 의견 제출...폰탄치료제 ‘... -
03 한미,“비만 넘어 항암으로 혁신”..미국암연... -
04 일양약품, 독감백신 ‘생후 6개월 이상 3세 ... -
05 동아제약, ‘얼박사 제로’ 출시 한 달 만에 2... -
06 미래의료혁신연구회,제약산업 구조 전환-글... -
07 차바이오텍,밀테니바이오텍과 차세대 항암 ... -
08 아미코젠, 농식품부 ‘국가 바이오소부장 국... -
09 일본 이세(ISE) 홀딩스, “한국 홍삼란 기술 ... -
10 아리바이오,경구 알츠하이머 치료제 임상3...










