뉴스
의료기기, 위해성 높을수록 허가 심사 어렵다
1등급은 즉시 신고가능, 2등급은 30일, 3·4등급은 65일간 허가 심사 진행
전세미 기자 │ jeonsm@yakup.com


입력 2017-06-09 06:31 수정 2017.06.09 09:45

|
박인숙 과장(식품의약품안전처 의료기기사업부)은 지난 8일 임페리얼팰리스호텔에서 열린 대한화상학회 학술대회에서 ‘의료기기 허가 심사와 최근 동향’을 주제로 강의를 진행했다.
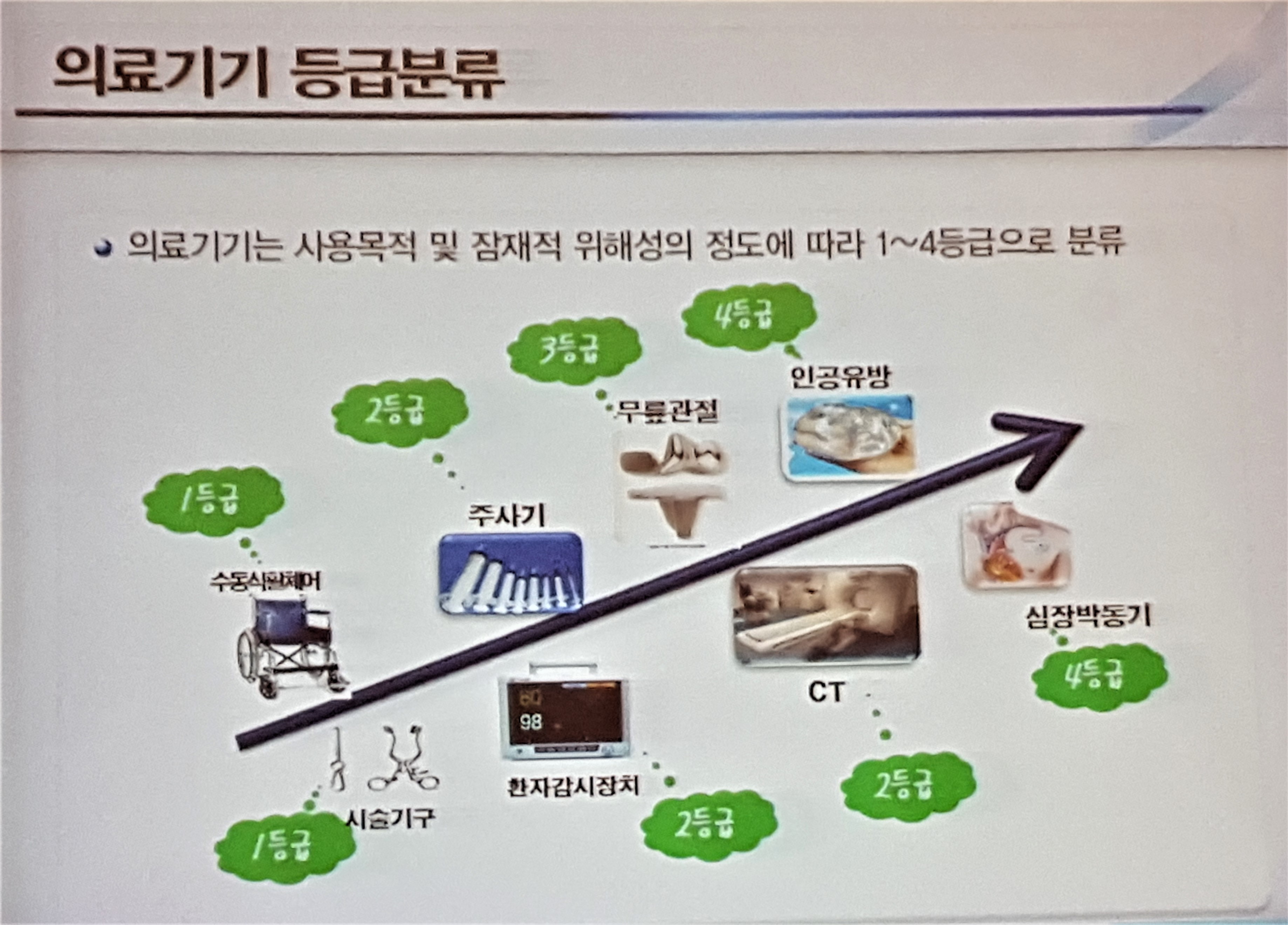
박 과장은 ‘현행 의료기기법에 따르면, ‘의료기기’란 사람 또는 동물에게 단독 또는 조합해 사용되는 기구·기계·장치·재료 또는 이와 유사한 제품으로, 의료기기로 명시되기 위해서는 일정 조건을 갖춰야 한다‘며 등급에 따른 의료기기 분류 제도를 소개했다.
◇의료기기의 분류 및 허가 과정
|
의료기기는 사람에게 직접 적용돼 인체에 해를 끼칠 수도 있는 만큼 허가 조건이 까다롭다. 허가 과정의 ‘서류 전형’에 해당하는 ‘기술문서 심사’ 과정은 허가 시 가장 먼저 거쳐야 하는 필수 관문이다.
의료기기 허가 시 제출해야 하는 ‘기술문서’는 ‘심사의뢰서’와 ‘구비서류’로 구성되며, 심사대상과 구비서류에 따라 ‘기술문서심사’와 ‘임상시험심사’로 구분된다.
이 중 기술문서심사는 의료기기의 성능 및 안전성 등 품질에 관한 자료를 바탕으로 심사하며, 의료기기 품목의 원자재, 구조, 사용목적, 사용방법, 작용원리, 사용시 주의사항, 시험규격 등이 주된 내용이다.
이렇게 기술문서 심사 과정을 통과한 후 제품은 신청한 등급에 따라 각각 다른 심사과정을 거친다. 의료기기는 등급에 따라 ‘신고, 인증, 허가’로 구분되기 때문이다.
1등급은 신고서 작성 후 바로 등록하면 ‘신고’로 이어진다. 2등급은 GMP 적합 인정서를 작성 후 기술문서와 첨부자료를 심사처에 제출하면 심사위탁 민간기관에서 25일간, 의료기기정보기술지원센터에서 5일간 심사를 진행한다. 이후 심사 기준을 통과하면 ‘인증’ 마크를 달게 된다.
3·4등급은 조금 다르다. 3·4급은 GMP 적합 인정서와 기술문서, 첨부자료 이외에도 임상시험 자료를 추가로 첨부해 제출해야 한다. 서류 제출이 끝나면 심사위탁 민간기관에서 55일, 의료기기정보기술지원센터에서 10일간 심사를 진행하는데 이 65일간 식품의약품안전평가원에서도 일괄 검토한다.
검토가 끝나면 임상시험 자료를 심사하는데 추가로 15일이 소요된다. 이 모든 절차를 통과해야만 ‘허가’를 받게 되는 것이다.
또한 2등급 의료기기 인증에 신청했다 하더라도 임상시험이 필요하거나 새로 출시된 기기면 식품의약품안전평가원에서 심사에 일부 관여한다.
◇의약품·의료기기의 임상시험
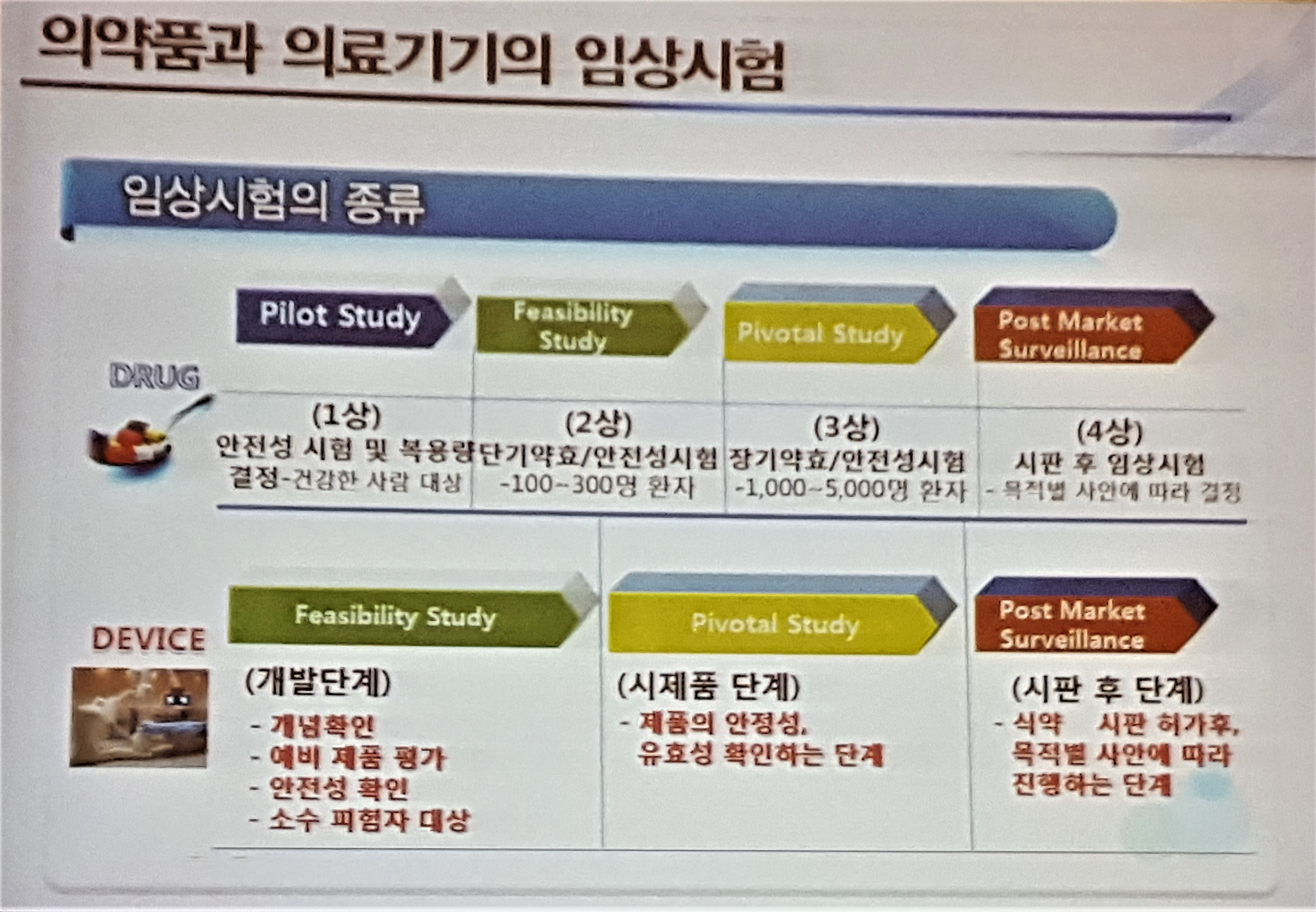
의약품과 의료기기의 임상시험은 신약 개발 과정에서 시행하는 임상시험과는 조금 다르다.
|
반면 의료기기의 임상시험은 총 3단계로 구분된다. △개발 단계-개념확인, 예비 제품 평가, 안전성 확인 △시제품 단계-제품의 안전성․유효성 확인 △시판 후 단계-식약 시판 허가 후 목적별 사안에 따라 진행의 과정을 거친다.
식약처가 공개한 자료에 따르면 의료기기 임상시험기관은 전국에 총 151곳이 지정돼있다(2016년 11월 기준). 151개 기관들은 대부분 의료기기와 의약품을 모두 취급해 시험하지만 소수의 일부 기관은 의료기기만을 대상으로 임상시험을 시행하는 것으로 나타났다.
◇창상피복재의 구분
식약처에서 규정하는 ‘창상피복재’는 1등급이 없다. 2등급 창상피복재는 ‘상처의 보호 및 삼출물 흡수, 1도 화상 적용’을 위해 지정됐다. 3등급은 ‘궤양 치료, 유착방지, 2도 화상 적용’에 쓰이며, 4등급은 ‘이식재와 같이 사용, 일시적인 피부대체재, 전층 부위 손상 및 3도 화상’을 위해 쓰이는 물질들이 포함된다.
전부 엇비슷해 보이는 창상피복재이지만, 그 안에서도 의약품과 의료기기, 의약외품으로 구분된다.
의료기기는 창상의 삼출물 흡수, 출혈 또는 체액손실 및 오염방지, 습윤환경 조성 등을 주요한 효과로 한다. 의약품은 의약품 성분에 의한 약리적인 치료를 위해 지정된 것이고, 의약외품은 ‘의약외품 범위 지정’에 따라 환부의 보존·보호·처치 등의 목적으로 사용된다. 안대, 붕대, 탄력붕대, 석고붕대, 원통형 탄력붕대, 거즈, 탈지면, 반창고가 여기에 속한다.
그러나 의약품과 의료기기 간 경계를 뚜렷하게 구분 짓기는 어렵다는 것이 식약처의 설명이다. 업체들이 하나의 주요 작용에 다른 작용을 더해 총 두 개 이상의 효능을 가진 의약품 및 의료기기를 개발하는 데 주력하고 있기 때문이다.
이에 식약처에서는 ‘의약품·의료기기 복합조합 품목’을 만들어 제품의 주요한 효과가 무엇인지를 우선 판단해 분류하고 있다. 박 과장은 “현재 복합조합 품목은 증가하는 추세이며, 앞으로도 더욱 증가할 것으로 전망된다”고 덧붙였다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 이모코그, ‘코그테라’ 출시 6개월 만 처방 1... -
02 디티앤씨바이오그룹, BIO KOREA 참가…현장 ... -
03 임성기재단, 2026년도 희귀난치성질환 연구... -
04 바이오시밀러도 규모 경제.. 미국 최대 제네... -
05 아이오니스 "RNA 치료제, 마지막 퍼즐 ‘독성... -
06 에피바이오텍, ‘보산진-애브비 바이오텍 이... -
07 캐나다 온타리오, K-바이오 북미 진출 전략... -
08 카나프테라퓨틱스,미국안과학회서 황반변성 ... -
09 바이오솔루션, '카티라이프' 중국 진출 전략... -
10 차바이오텍,판교 제2테크노밸리 CGB 대규모 ...










