뉴스
지난해 신약 허가 25개중 국산제품은 2개 불과
한미약품 올리타정 2품목만 국산, 항악성종양제 8품목으로 최다
김용주 기자 │ yjkim@yakup.com


입력 2017-01-18 06:30 수정 2017.01.18 08:29
|
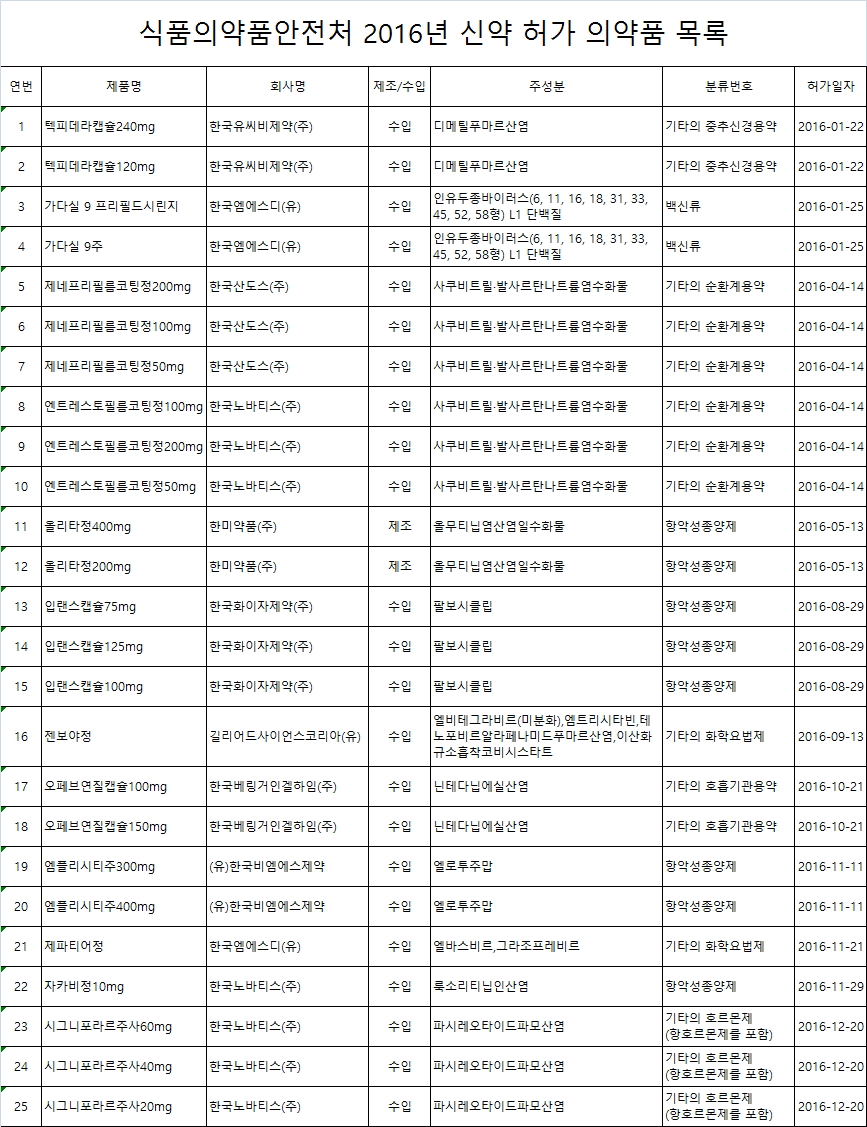
식품의약품안전처로부터 지난해 신약으로 허가받은 의약품은 총 25개인 것으로 나타났다.
하지만 국내 제약사가 개발해 허가를 받은 신약은 한미약품의 비소성폐암치료제 '올리타정 200mg, 400mg' 등 2개에 불과했다.
식품의약품안전처가 지난해 허가한 신약은 9개사 25개 품목으로 집계됐다. 이중 한미약품의 항악성종양제 '올리타정 200mg, 400mg‘ 2품목을 제외하면 수입된 제품이 신약으로 허가를 받은 것으로 나타났다.
회사별로는 한국노바티스가 항악성종양제 '자카비카정10mg' 등 7품목으로 가장 많은 제품을 허가받았고, 한국산도스 한국화이자제약 한국엠스디 등이 각각 3품목의 허가를 받은 것으로 집계됐다.
분류번호별로는 항악성종양제가 8품목으로 가장 많았다. 한국화이자의 ‘입랩스캡슐’, 한국비엠에스제약의 ‘엠플리시티주’, 한국노바티스의 ‘자카비정’, 한미약품의 ‘올리타정’ 등이 항악성종양제로 허가받은 의약품이다.
한국산도스의 '제네프리필름코팅정', 한국노바티스의 '엔트레스토필름코팅정 등 6개 품목은 기타의 순환계용약으로 신약 허가를 받았다.
유전자재조합의약품은 총 4품목이 신약으로 허가를 받았다. 한국엠에스디의 백신 '가다실 9 프리필드시린지' '가다실 9주'등 2품목, 한국비엠에스제약의 '엠플리시티주 300mg, 400mg' 등 2품목이 유전자재조합 의약품이다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 삼성바이오로직스 파업 2일차…일부 공정 중... -
02 삼성바이오로직스 "교섭 지속했지만 합의 실... -
03 "K-제약바이오, 왜 아직 ‘블록버스터 신약’ ... -
04 "오가노이드 글로벌 생태계, 한국에 모인다"... -
05 파인트리테라퓨틱스, 아스트라제네카와 EGFR... -
06 셀트리온, 유럽 EMA에 ‘허쥬마SC’ 제형 추가... -
07 K-오가노이드 컨소시엄, 2026년 정기총회 개... -
08 한미사이언스, 1분기 경영 실적 발표… 전년... -
09 에스티젠바이오, ‘비티젠’으로 사명 변경… ... -
10 한미약품, 1분기 매출 3929억 달성… 원외처...










