뉴스
신약 허가 시 완제의약품-원료의약품 실사 연계
식약처, 완제 GMP 및 DMF 실사 일정 연계 공개
신은진 기자 │ ejshin@yakup.com


입력 2016-03-29 06:00 수정 2016.03.29 07:02
|
신약 허가 시 제조업소 GMP 실사 일정이 보다 효율적으로 개선될 예정이다.
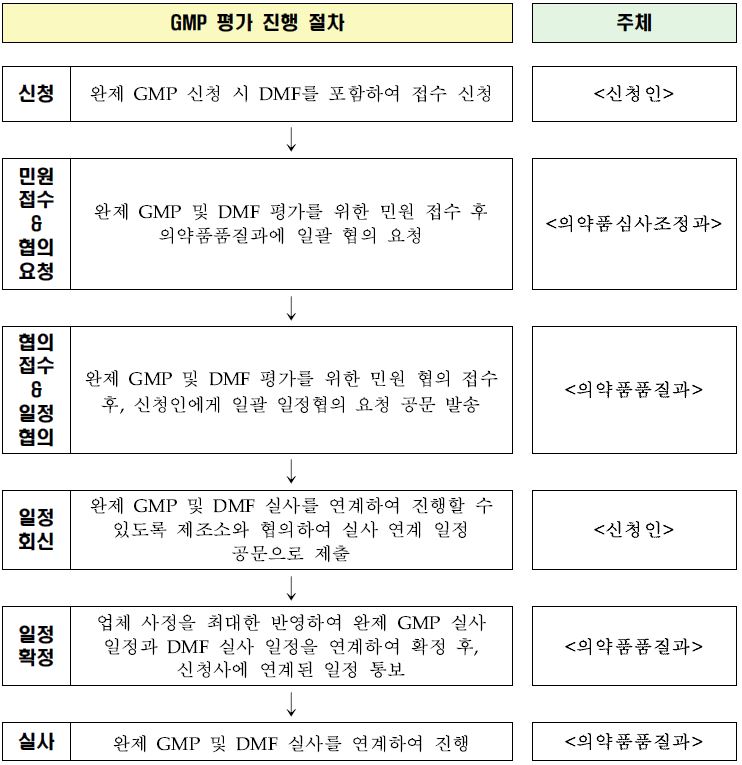
식품의약품안전처는 28일 신약 허가 시 완제의약품과 원료의약품 제조업소에 대한 실태조사 일정을 연계한다고 밝혔다.
이에 따라 신약 허가 시 DMF를 포함한 완제 GMP 신청이 가능해진다.
접수가 이뤄진 후 식약처와 업체 간 일정조율이 진행되며, 식약처는 업체사정을 최대한 고려해 완제 GMP와 DMF 실사 연계일정을 최종 결정한다는 방침이다.
식약처는 신약 허가 시 완제의약품과 원료의약품 실사일정 연계로 효율적인 GMP평가가 이뤄질 수 있을것으로 기대하고 있다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 셀리드,코로나19 예방백신 임상2상 시험 IND... -
02 국가신약개발사업단,투자 적격 기준 -향후 ... -
03 GC녹십자, 1Q 매출 13.5%↑4355억원-영업익 ... -
04 한미약품, 2030 목표 위한 ‘혁신-지속-미래-... -
05 북경한미, 사상 첫 4000억 매출 돌파…지속 ... -
06 40년 만 허가 새 멀미 치료제 미국서 공급 ... -
07 메지온, 유럽소아심장학회서 'JURVIGO' 임상... -
08 [약업분석]HLB그룹 연구개발비 확대·자산인... -
09 미국 '트럼프RX’ 참여 17개 제약사 지난해 ... -
10 유한양행, IWGGD 2026서 고셔병 치료제 'YH3...










