테클리스타맙·엘라나타맙 등 다발골수종 신약 포함
위암·요로상피암·식도암 치료제 급여기준도 새로 설정

|
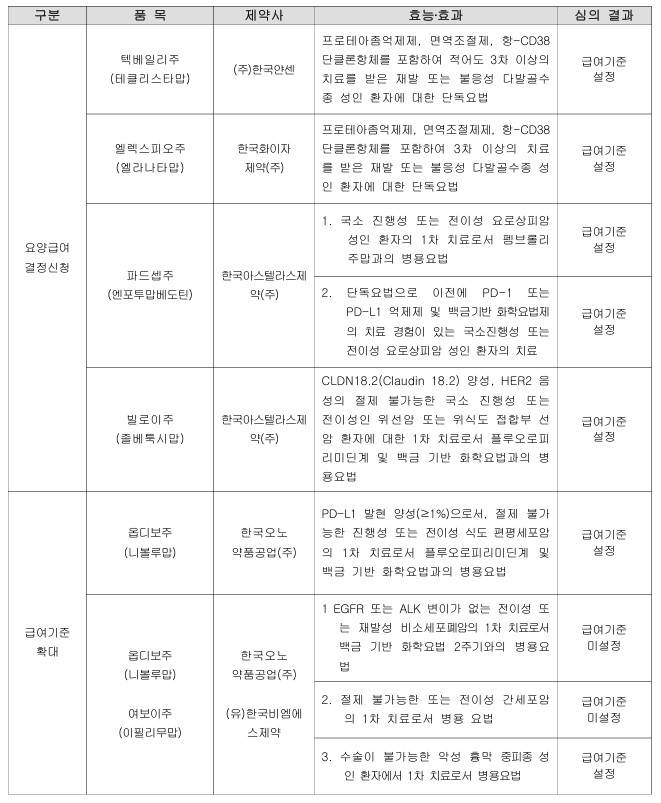
건강보험심사평가원은 29일 제8차 암질환심의위원회를 열고 암환자 대상 신약의 요양급여 기준을 심의한 결과, 6개 품목(7개 적응증)의 급여기준을 새로 설정하고 일부 적응증에 대해 확대 적용하기로 했다.
이번 심의에서는 재발·불응성 다발골수종을 비롯해 위암, 요로상피암, 식도암 등 주요 고형암 치료제들이 대거 급여 항목에 포함되며 항암 치료 접근성이 한층 넓어졌다.
다발골수종 신약, 급여 장벽 넘어 첫 통과
이번 암질심 통과 품목 가운데 가장 주목받은 약제는 △텍베일리주(테클리스타맙, 한국얀센)와 △엘렉스피오주(엘라나타맙, 한국화이자제약)다.
두 약제는 프로테아좀억제제·면역조절제·항-CD38 단클론항체 치료를 모두 받은 3차 이상 재발 또는 불응성 다발골수종 성인 환자를 대상으로 하는 단독요법으로 급여기준이 설정됐다.
이들 모두 이중항체(bispecific antibody) 기전의 혁신 치료제로, FDA와 식약처에서 2상 임상결과를 토대로 신속 승인(Fast Track)을 받은 약제다.
그동안 암질심은 ▲3상 확증 임상 부재 ▲장기 추적 데이터 부족 등을 이유로 급여 결정을 보류해 왔으나, 이번 회의에서 임상적 유용성과 환자 수요를 인정받으며 급여 진입의 물꼬를 텄다.
파드셉·빌로이, 고형암 첫 진입…“치료 공백 해소”
△파드셉주(엔포투맙베도틴, 한국아스텔라스제약)는 ①국소 진행성 또는 전이성 요로상피암의 1차 치료에서 펨브롤리주맙 병용요법, ②PD-1/PD-L1 억제제 및 백금기반 화학요법 경험 환자의 단독요법 두 적응증 모두 급여기준이 설정됐다.
파드셉은 요로상피암 영역에서 약 30년 만에 등장한 최초의 항체-약물 접합체(ADC)로, 국내에서는 2023년 허가 후 2024년 급여심의에 연이어 도전해왔다. 이번 결정으로 1차 병용요법까지 급여가 인정되며 실질적 치료 접근성이 확보됐다.
이와 함께 같은 회사의 △빌로이주(졸베툭시맙) 역시 암질심을 통과했다.
CLDN18.2 양성·HER2 음성의 절제 불가능한 국소 진행성 또는 전이성 위선암 및 위식도접합부 선암에서 플루오로피리미딘계 및 백금 기반 화학요법 병용요법으로 급여기준이 설정됐다.
빌로이는 CLDN18.2 표적을 겨냥한 세계 최초 신약으로, 기존 HER2 음성 위암에서 선택지가 부족했던 환자에게 새로운 치료 옵션이 될 전망이다.
옵디보, 식도암·중피종 통과…폐암·간암은 ‘보류’
△옵디보주(니볼루맙, 한국오노약품공업)는 PD-L1 발현(≥1%) 식도 편평세포암의 1차 치료 병용요법에 대한 급여기준이 확대됐다.
또한 옵디보와 여보이주(이필리무맙, 한국BMS제약) 병용요법 중 수술이 불가능한 악성 흉막중피종 성인 환자의 1차 치료 적응증 역시 급여기준이 설정됐다.
다만 비소세포폐암(EGFR/ALK 변이 음성) 및 절제 불가능한 간세포암의 1차 병용요법은 급여기준 미설정으로 결론났다.
-
01 노바렉스, 620억원 투입 오송 2공장 신축 -
02 암 신약 4종 급여기준 신설…‘옵디보+여보이’... -
03 약준모 제7대 회장에 박현진 약사 당선…재선... -
04 파마재니스텍 홍성창 대표이사, 2025 혁신특... -
05 한미사이언스…3분기 영업익 75.2% 증가 -
06 필수약 공급중단, 상시 대응체계 필요…협의... -
07 파인트리테라퓨틱스, 670억원 시리즈B 유치 ... -
08 지씨셀, 중국 IASO와 'CAR-T 푸카소' 국내 ... -
09 파미셀, CPHI 프랑크푸르트서 글로벌 협력 ... -
10 한국당뇨협회,11월 9일 '블루런'..셀럽 참여...











