
|
해당 임상 시험은 재발성/불응성 고형암 환자를 대상으로 지아이셀의 동종유래 NK세포치료제인 T.O.P. NK와 지아이이노베이션의 차세대 면역항암제인 GI-101A 병용요법 안전성 및 잠재적 유효성을 평가하기 위한 국내 1/2a상 임상시험이다. 양사는 향후 추가적인 협업을 통해 T.O.P. NK와 GI-102의 병용요법 임상도 돌입할 예정이다.
T.O.P. NK는 대량배양이 가능하고 종양 타깃능과 암세포 살상효율을 극대화한 차세대 NK세포치료제로, 현재 재발성/불응성 고형암 및 혈액암 환자를 대상으로 단독요법 임상 1상을 진행 중이다.진
임상 1상 중간 결과에 따르면 표준치료에 실패한 비호지킨 림프종 환자에 T.O.P. NK를 3회 투약 후 첫번째 종양평가를 수행한 결과 완전관해(Complete response, CR)를 확인했다. 또한최소 3번의 표준치료에 실패한 직장암 환자 4명 중 3명에서 6개월 이상 투약이 진행됐으며, 이중 2명에서는 종양이 감소하는 안정적병변(SD)을 확인했다. 지아이셀은 NK세포치료제 단독요법 임상임에도 재발성 림프종에서 효능을 확인했으며, 특히 직장암 3차 표준치료의 무진행 생존기간 (median Progression-free survival, mPFS)이 약 2개월인 점을 고려하면 직장암에서도 고무적인 결과를 보여주었다고 설명했다.
GI-101A는 ‘CD80’과 ‘IL-2 변이체’ 기능을 동시에 가진 이중융합단백질로 IL-2부위는 면역세포의 증식 및 활성화에 관여하고, CD80은 암세포를 공격하는 면역세포를 억제하는 수용체인 CTLA4를 차단하는 역할을 한다. 현재 면역항암제 키트루다와 병용요법으로 국내와 미국에서 임상 1/2상 진행중이다.
해당 임상에서 GI-101A가 면역항암제에 내성이 있는 암환자의 면역세포를 무진행 생존기간을 현저히 증가시킴을 확인했다. 또 GI-102는 엔지니어링을 통해 GI-101A대비 알파 수용체 결합력을 떨어뜨린 파이프라인으로 최근 기존 치료법에 불응 또는 재발한 흑색종 환자를 대상으로 43%의 객관적반응률(ORR)과 면역세포 수를 평균 7배 증가시키는 임상 1/2a상 결과를 발표했다.
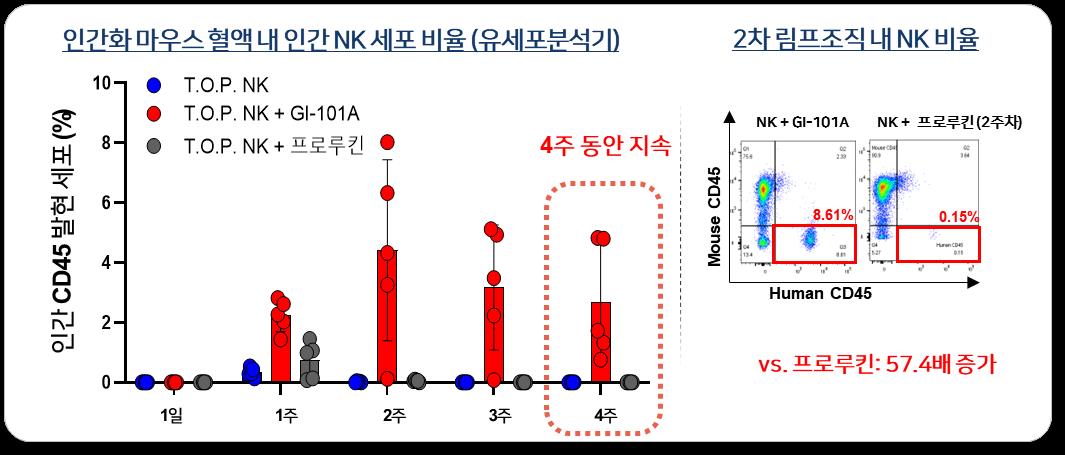
양사에 따르면 인간화 마우스를 이용한 비임상 시험에서 GI-101A 또는 GI-102와 T.O.P. NK의 병용투여 시, T.O.P. NK의 체내 지속성이 1개월간 유지되고 T.O.P. NK 단독투여 대비 항암효능이 증가함을 확인했다. 지아이셀은 이러한 결과를 바탕으로 GI-101A/GI-102와의 병용요법에서 T.O.P. NK의 투여 용량을 단독요법 대비 수배에서 수십배 낮춤으로써 생산원가를 줄여 상업성을 높일 수 있을 것으로 기대하고 있다.
장명호 지아이셀 최고임상과학고문은 “최근 첨생법 개정안 국회 본회의 통과로 말기암 환자 뿐만 아니라 초기암 및 수술 후 환자분들도 세포∙유전자 치료를 받을 수 있는 길이 열렸다”며 “GI-101A/GI-102와 T.O.P. NK 병용요법 성공적 개발을 통해 더 많은 환자분들이 혜택을 보실 수 있도록 최선을 다하겠다”고 말했다.
-
01 LG화학, 미국 프론티어-메디신즈 항암제 후... -
02 랩지노믹스,유투의료재단과 검체위수탁사업 ... -
03 삼성제약, '삼성로수바스타틴정20밀리그램' ... -
04 HK이노엔,아토피 피부염 치료제 임상1b상 I... -
05 아이빔테크놀로지,미국 CSHL·프랑스 IPAM 등... -
06 지오영 그룹, 창사 이래 첫 매출 5조 돌파 -
07 지투지바이오, SIRS서 3대 CNS 질환 타깃 '... -
08 일라이 릴리, 영국 센테사 파마 최대 78억달... -
09 '거점도매' 공방 확산…대웅, 공급망 투명성 ... -
10 "생존 전쟁" 선포…유통협회, 대웅 '거점도매...











