뉴스
[인터뷰]이뮨온시아 “항암신약 성공, 골대 앞에 서다”…IMC-001 2상서 '완전관해' 확인
김흥태 대표, 파이프라인 비임상·임상단계에서 우수성 입증…'기술이전·상장' 자신
권혁진 기자 │ hjkwon@yakup.com


입력 2022-05-11 06:00 수정 2022.05.12 09:19
몇 년 전만 해도 항암제를 떠올리면, 화학항암제를 먼저 떠올렸다. 그러나 이제 대세는 면역항암제로 완전히 기울어졌다. 면역항암제는 인체의 면역 시스템을 기반으로 암세포를 사멸해 기존 항암제에서 발생하던 부작용이 대폭 감소했다. 이와 더불어 초기 개발된 면역항암제의 낮은 효과를 기술로써 극복해 항암효과를 대폭 끌어올렸다.
이뮨온시아의 면역항암제도 이러한 특징이 있다. IMC-001는 ADCC 기능이 활성화돼 있어, 더 강력한 효과를 나타낸다. 특히 임상 단계에 있는 다른 경쟁 면역항암제들과 달리 희귀암을 타깃으로 해, 임상 성공 시 미충족 의료수요를 충족시킬 수 있는 First-in-class로 기대를 받고 있다. 또 다른 면역항암제 IMC-002는 적혈구 응집(RBC Binding)을 거의 보이지 않아, 안전성이 뛰어나다. 이러한 우수성을 인정받아 중국의 면역항암제 개발 전문 기업에 기술수출을 하는 성과를 이뤄냈다.
또한 한국투자증권을 주관사로 선정하고, 기술 특례 방식으로 올 하반기 코스닥 상장 목표를 밝혔다. 이에 약업닷컴은 이뮨온시아 김흥태 대표이사에게 이뮨온시아의 임상개발 현황과 사업전략에 대해 전해 들었다.
Q. 이뮨온시아 소개 부탁드린다.
이뮨온시아는 지난 2016년 유한양행과 미국 나스닥 상장사인 소렌토 테라퓨틱스가 합작해 설립한 면역항암제 신약개발 바이오텍이다. 현재 CD47 항체 후보물질 ‘IMC-002’와 PD-L1 항체 후보물질 ‘IMC-001’ 등, 유망 신약후보 파이프라인을 구축했고, IMC-002와 IMC-001은 임상단계에 진입했다. 또한 내년 IND 승인을 목표로 전임상 개발 중인 ‘IMC-201(PDL1xCD47 이중항체)’와 여러 신약후보물질이 전임상 단계에서 연구 개발 중이다.
특히 지난해 3월에는 중국 3D메디슨에 ‘IMC-002’의 중국지역 개발권리를 총 5,400억원에 기술이전 계약을 성사시켰고, 또 지난해 12월에는 프리미어파트너스 등으로부터 245억원 규모의 Pre-IPO 투자를 유치하는 성과도 이뤄냈다.
Q. IMC-001(PD-L1) 소개와 작용기전 특징은.
IMC-001은 T세포에서 발현되는 PD-1과 암세포 표면에서 발현하는 PD-L1 간 결합을 강력하게 저해함으로써, T세포의 항암 활동을 활성화시키는 기전을 가진다. 또한 IMC-001은 Human IgG1을 사용하므로 Fc effector 기능을 유지하고 있다. 이에 따라 IgG4를 사용하는 키트루다·옵디보 및 Engineered IgG1을 사용하는 티센트릭·임핀지 등과 달리, ADCC(antibody-dependent cellular cytotoxicity) 기능이 활성화돼 있어, NK세포치료제 등과 병용 시 높은 효과를 나타낼 것으로 기대된다.
Q. IMC-001 국내 임상 1상 결과는.
전이성/국소 진행성 고형암 환자 15명을 대상으로 안전성 및 내약성 검증을 완료했다. 용량제한독성은 관찰되지 않았고, 3등급 이상의 독성도 전혀 없었다. 특히 일부 고형암에서는 유효성을 확인했는데, PR(Partial Response)을 보인 직장암 환자 1명은 반응지속 기간(DOR)이 무려 14개월이나 됐고, 담도암 환자 3명에서는 모두 SD(Stable Disease)가 관찰됐다.
Q. IMC-001 임상 1상 결과 기반으로 2·3상 최종 결과를 예측해 본다면.
임상 1상에서 20mg/kg까지 MTD(Maximal Tolerated Dose)에 도달하지 않았으나, 약동학 및 약력학 데이터를 기반으로 20mg/kg을 2상 권장용량(RP2D)으로 결정했고, 이에 따라 안전성 및 내약성은 우수할 것으로 예측된다. 특히 직장암 환자 1명에서 PR과 담도암 환자 3명 모두에서 질병조절률 100%를 보였던바, 소화기계 암종에 단독 및 병용 시, 우수한 효과가 예상된다.
Q. IMC-001 국내 임상 2상 진행 현황과 중간 결과는.
PD-(L)1 면역항암제의 승인은 시장성이 큰 주요 암 위주로 돼 있어, 주요 암은 포화상태지만, 희귀암의 승인과 임상시험은 여전히 사각지대에 놓여 있다. 임상 2상에서는 미충족 수요가 큰 희귀 암인 NK/T 세포 림프종을 적응증으로 선정해 유효성과 안전성을 평가하고 있다.
현재까지 8명의 환자가 등록됐으며, 임상시험 과정에서 중대한 약물 이상반응은 없었다. 특히 올해 4월 기준으로 총 등록환자 9명 중 평가 가능한 4명의 환자에서 모두 완전관해가 확인됐고, 현재까지 지속적인 치료 효과를 유지하고 있다. 최근 국내에서 임상 기관 4곳을 추가해 환자등록 속도를 올리고 있다.
▲IMC-002 비임상시험 데이터
Q. IMC-002(CD47) 작용기전과 경쟁력은.
IMC-002는 암세포 표면에서 발현하는 CD47과 대식세포 표면의 SIRPα간 결합 ('Don’t eat me' 신호)을 저해함으로써 대식세포의 암세포 포식을 활성화시키는 기전을 갖고 있다. 전임상 단계에서 경쟁약물 대비 우수한 안전성과 PK 프로파일이 확인됐고, 이러한 우수한 결과를 바탕으로 지난해 3월, 중국 3D메디슨에 한화 약 5,400억원 규모로 기술수출을 했다.
Q. IMC-002 비임상시험 결과는.
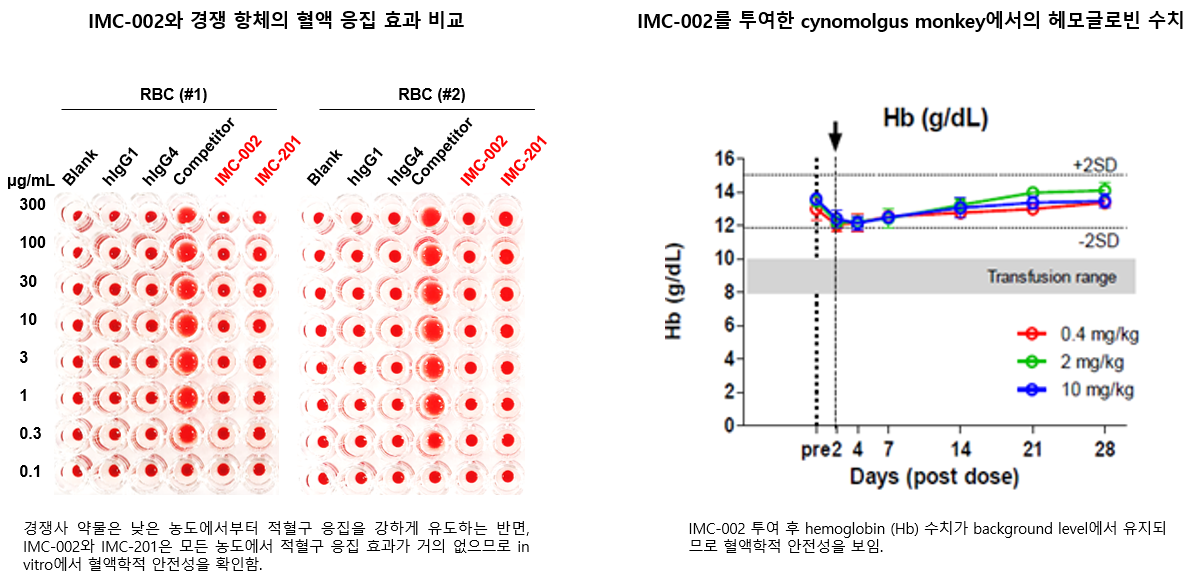
CD47은 적혈구 또는 혈소판 등의 정상세포에도 발현돼 있어, 경쟁약물들은 빈혈(Anemia)이나 혈소판 감소(Thrombocytopenia) 등의 부작용을 동반하는 경우가 많다. 하지만 IMC-002은 in vitro에서 적혈구 응집을 거의 보이지 않았고, 원숭이 독성시험에서도 용량을 늘려도 혈소판 수치가 거의 떨어지지 않아, 경쟁약물들과 비교했을 때 안전성 측면에서 확실한 경쟁우위를 나타냈다.
이에 따라 antigen sink가 최소화되기 때문에 PK 측면에서도 타사 약물대비 경쟁우위를 가질 것으로 보인다. 실제 현재 임상 진행 중인 상당수의 타사 약물들은 주 1회 투여지만, IMC-002는 현재 주 2회 투여로 진행되고 있다.
Q. IMC-002 미국과 한국 임상시험 현황은.
미국 임상 1상의 경우, 고형암 및 림프종 환자들을 대상으로 용량상승(Dose Escalation) 1a상을 진행 중이다. 현재까지 용량제한 독성 등의 문제는 없었다. 그러나 COVID-19의 장기화로 환자 모집에 어려움을 겪어 임상이 지연되고 있다. 또한 임상 시료의 수집 및 분석에서 해외 CRO 및 분석 Lab을 이용할 수밖에 없다 보니 아무래도 quality control에 어려움이 있다.
이에 따라 임상 quality 제고와 바이오마커 분석, 미충족수요가 큰 고형암에서 임상 1상의 완료를 가속화해, 임상 2상 용량(RP2D)을 신속히 결정하기 위해 한국에서 새롭게 임상 1상을 진행하고 있다. 국내 임상 1상은 올해 3월 식약처로부터 IND를 승인받아 5월부터 삼성서울병원에서 환자등록을 진행 중이다. 임상시험의 디자인 설계 방식 Phase 1a에서 2주 간격, 정맥 투여하며 3+3 방식으로 디자인했고, 15명 환자가 등록 예정이다.
Q. IMC-001 기술이전 등 사업화 계획은.
IMC-001은 해외 기술이전과 국내 상용화를 동시에 추진하는 투 트랙 전략을 추진하고 있다. 해외 기술이전은 NK/T세포 림프종 치료제에 대한 미충족 의료수요가 높은 중국을 1순위로 추진하고 있고, 진행 중인 NK/T세포 림프종 2상에서 유의한 효능 데이터가 확보되는 올해 말부터 기술이전 기회가 본격화될 것으로 예상된다.
국내에서는 현재 임상개발 중인 NK/T세포 림프종과 하반기 임상개시 예정인 TMB-high 고형암을 적응증으로, 오는 2026년 식약처 승인을 목표로 하고 있다. 현재 국내에서는 해당 암종에서 승인받은 면역항암제가 전무하기 때문에, 당사가 식약처 승인을 받게 되면 2개 적응증에서 국내 first-in-class 면역항암 치료제가 되고, 실제 상업화 단계에서는 당사 1대 주주인 유한양행과 협업을 통해 시너지를 극대화할 계획이다.
Q. IMC-002 기술이전 가능성은.
올해 말까지 IMC-002의 용량 상승(Dose escalation) 1a상을 완료하고, 내년부터는 다른 약물과 병용하는 용량확장(Dose expansion) 1b상을 개시해 24년에 일부 암종에서 POC 데이터 확보를 목표로 하고 있다.
CD47 시장은 2020년 이후 길리어드, 화이자, 애브비 등 빅파마들 주도로 대형 M&A와 Licensing 계약이 연달아 이뤄지면서 크게 주목을 받았고, 항암제 분야의 글로벌 메이저들의 추가투자 가능성이 매우 높다. 현재 전 세계적으로 이뮨온시아를 포함한 9개 기업에서 임상단계 개발을 진행 중이고, 이 중 M&A와 기술이전을 통해 파트너링이 완료된 3개사를 제외하면, 당사를 포함한 6개 회사가 'Next Big Deal'의 주인공이 될 가능성이 높다.
비임상에서 보여준 우수한 Safety/PK 프로파일을 임상에서 검증하게 되는 올해 말부터 글로벌 기술이전 기회가 본격화될 것으로 예상하고 있고, 병용 1b상을 통해 일부 암종에서의 POC데이터를 확보하게 되는 2024년에는 더욱 높은 가치로 글로벌 기술이전 기회가 있을 것으로 전망된다.
Q. 이외 개발 중인 유망 파이프라인은.
지난 4월 AACR에서 뜨거운 관심을 받았던 IMC-201(IOH-001)은 PD-L1 및 CD47 타깃의 이중항체로, 선천면역 (대식세포의 암세포 포식)과 후천면역(T세포의 암세포 살상)을 동시에 활성화하는 기전을 가졌다. 내년 하반기 IND 신청 및 승인을 목표로 세포주개발 및 공정개발 등 전임상 개발에 매진하고 있다.
이 외에도 LAG-3 단클론 항체(IMC-003)가 전임상 단계까지 개발됐고, 유한양행과 공동개발 중인 이중항체(IOH-003)와 레고켐바이오사이언스와 공동개발 중인 AIC(면역조절항체 결합체, IOH-004)가 올해 중으로 Lead 단계에 진입할 예정이다.
Q. 이뮨온시아의 비전과 마지막으로 전하고 싶은 말씀 부탁드린다.
전 세계 암환자에게 안전하고 효과적인 새로운 면역치료제를 제공하는 것을 최우선으로 하고 있다. 면역항암제 개발에 성공해, 국내 최고의 면역항암제 개발 선도기업이 될 것이며, 이를 통해 암환자들에게 혜택을 주고, 국내 면역항암제 연구 활성화와 국가재정에도 기여할 수 있는 기업이 되도록 최선을 다할 것이다.

|
또한 한국투자증권을 주관사로 선정하고, 기술 특례 방식으로 올 하반기 코스닥 상장 목표를 밝혔다. 이에 약업닷컴은 이뮨온시아 김흥태 대표이사에게 이뮨온시아의 임상개발 현황과 사업전략에 대해 전해 들었다.
Q. 이뮨온시아 소개 부탁드린다.
이뮨온시아는 지난 2016년 유한양행과 미국 나스닥 상장사인 소렌토 테라퓨틱스가 합작해 설립한 면역항암제 신약개발 바이오텍이다. 현재 CD47 항체 후보물질 ‘IMC-002’와 PD-L1 항체 후보물질 ‘IMC-001’ 등, 유망 신약후보 파이프라인을 구축했고, IMC-002와 IMC-001은 임상단계에 진입했다. 또한 내년 IND 승인을 목표로 전임상 개발 중인 ‘IMC-201(PDL1xCD47 이중항체)’와 여러 신약후보물질이 전임상 단계에서 연구 개발 중이다.
특히 지난해 3월에는 중국 3D메디슨에 ‘IMC-002’의 중국지역 개발권리를 총 5,400억원에 기술이전 계약을 성사시켰고, 또 지난해 12월에는 프리미어파트너스 등으로부터 245억원 규모의 Pre-IPO 투자를 유치하는 성과도 이뤄냈다.
Q. IMC-001(PD-L1) 소개와 작용기전 특징은.
IMC-001은 T세포에서 발현되는 PD-1과 암세포 표면에서 발현하는 PD-L1 간 결합을 강력하게 저해함으로써, T세포의 항암 활동을 활성화시키는 기전을 가진다. 또한 IMC-001은 Human IgG1을 사용하므로 Fc effector 기능을 유지하고 있다. 이에 따라 IgG4를 사용하는 키트루다·옵디보 및 Engineered IgG1을 사용하는 티센트릭·임핀지 등과 달리, ADCC(antibody-dependent cellular cytotoxicity) 기능이 활성화돼 있어, NK세포치료제 등과 병용 시 높은 효과를 나타낼 것으로 기대된다.
Q. IMC-001 국내 임상 1상 결과는.
전이성/국소 진행성 고형암 환자 15명을 대상으로 안전성 및 내약성 검증을 완료했다. 용량제한독성은 관찰되지 않았고, 3등급 이상의 독성도 전혀 없었다. 특히 일부 고형암에서는 유효성을 확인했는데, PR(Partial Response)을 보인 직장암 환자 1명은 반응지속 기간(DOR)이 무려 14개월이나 됐고, 담도암 환자 3명에서는 모두 SD(Stable Disease)가 관찰됐다.
Q. IMC-001 임상 1상 결과 기반으로 2·3상 최종 결과를 예측해 본다면.
임상 1상에서 20mg/kg까지 MTD(Maximal Tolerated Dose)에 도달하지 않았으나, 약동학 및 약력학 데이터를 기반으로 20mg/kg을 2상 권장용량(RP2D)으로 결정했고, 이에 따라 안전성 및 내약성은 우수할 것으로 예측된다. 특히 직장암 환자 1명에서 PR과 담도암 환자 3명 모두에서 질병조절률 100%를 보였던바, 소화기계 암종에 단독 및 병용 시, 우수한 효과가 예상된다.
Q. IMC-001 국내 임상 2상 진행 현황과 중간 결과는.
PD-(L)1 면역항암제의 승인은 시장성이 큰 주요 암 위주로 돼 있어, 주요 암은 포화상태지만, 희귀암의 승인과 임상시험은 여전히 사각지대에 놓여 있다. 임상 2상에서는 미충족 수요가 큰 희귀 암인 NK/T 세포 림프종을 적응증으로 선정해 유효성과 안전성을 평가하고 있다.
현재까지 8명의 환자가 등록됐으며, 임상시험 과정에서 중대한 약물 이상반응은 없었다. 특히 올해 4월 기준으로 총 등록환자 9명 중 평가 가능한 4명의 환자에서 모두 완전관해가 확인됐고, 현재까지 지속적인 치료 효과를 유지하고 있다. 최근 국내에서 임상 기관 4곳을 추가해 환자등록 속도를 올리고 있다.
|
▲IMC-002 비임상시험 데이터
Q. IMC-002(CD47) 작용기전과 경쟁력은.
IMC-002는 암세포 표면에서 발현하는 CD47과 대식세포 표면의 SIRPα간 결합 ('Don’t eat me' 신호)을 저해함으로써 대식세포의 암세포 포식을 활성화시키는 기전을 갖고 있다. 전임상 단계에서 경쟁약물 대비 우수한 안전성과 PK 프로파일이 확인됐고, 이러한 우수한 결과를 바탕으로 지난해 3월, 중국 3D메디슨에 한화 약 5,400억원 규모로 기술수출을 했다.
Q. IMC-002 비임상시험 결과는.
CD47은 적혈구 또는 혈소판 등의 정상세포에도 발현돼 있어, 경쟁약물들은 빈혈(Anemia)이나 혈소판 감소(Thrombocytopenia) 등의 부작용을 동반하는 경우가 많다. 하지만 IMC-002은 in vitro에서 적혈구 응집을 거의 보이지 않았고, 원숭이 독성시험에서도 용량을 늘려도 혈소판 수치가 거의 떨어지지 않아, 경쟁약물들과 비교했을 때 안전성 측면에서 확실한 경쟁우위를 나타냈다.
이에 따라 antigen sink가 최소화되기 때문에 PK 측면에서도 타사 약물대비 경쟁우위를 가질 것으로 보인다. 실제 현재 임상 진행 중인 상당수의 타사 약물들은 주 1회 투여지만, IMC-002는 현재 주 2회 투여로 진행되고 있다.
Q. IMC-002 미국과 한국 임상시험 현황은.
미국 임상 1상의 경우, 고형암 및 림프종 환자들을 대상으로 용량상승(Dose Escalation) 1a상을 진행 중이다. 현재까지 용량제한 독성 등의 문제는 없었다. 그러나 COVID-19의 장기화로 환자 모집에 어려움을 겪어 임상이 지연되고 있다. 또한 임상 시료의 수집 및 분석에서 해외 CRO 및 분석 Lab을 이용할 수밖에 없다 보니 아무래도 quality control에 어려움이 있다.
이에 따라 임상 quality 제고와 바이오마커 분석, 미충족수요가 큰 고형암에서 임상 1상의 완료를 가속화해, 임상 2상 용량(RP2D)을 신속히 결정하기 위해 한국에서 새롭게 임상 1상을 진행하고 있다. 국내 임상 1상은 올해 3월 식약처로부터 IND를 승인받아 5월부터 삼성서울병원에서 환자등록을 진행 중이다. 임상시험의 디자인 설계 방식 Phase 1a에서 2주 간격, 정맥 투여하며 3+3 방식으로 디자인했고, 15명 환자가 등록 예정이다.
Q. IMC-001 기술이전 등 사업화 계획은.
IMC-001은 해외 기술이전과 국내 상용화를 동시에 추진하는 투 트랙 전략을 추진하고 있다. 해외 기술이전은 NK/T세포 림프종 치료제에 대한 미충족 의료수요가 높은 중국을 1순위로 추진하고 있고, 진행 중인 NK/T세포 림프종 2상에서 유의한 효능 데이터가 확보되는 올해 말부터 기술이전 기회가 본격화될 것으로 예상된다.
국내에서는 현재 임상개발 중인 NK/T세포 림프종과 하반기 임상개시 예정인 TMB-high 고형암을 적응증으로, 오는 2026년 식약처 승인을 목표로 하고 있다. 현재 국내에서는 해당 암종에서 승인받은 면역항암제가 전무하기 때문에, 당사가 식약처 승인을 받게 되면 2개 적응증에서 국내 first-in-class 면역항암 치료제가 되고, 실제 상업화 단계에서는 당사 1대 주주인 유한양행과 협업을 통해 시너지를 극대화할 계획이다.
Q. IMC-002 기술이전 가능성은.
올해 말까지 IMC-002의 용량 상승(Dose escalation) 1a상을 완료하고, 내년부터는 다른 약물과 병용하는 용량확장(Dose expansion) 1b상을 개시해 24년에 일부 암종에서 POC 데이터 확보를 목표로 하고 있다.
CD47 시장은 2020년 이후 길리어드, 화이자, 애브비 등 빅파마들 주도로 대형 M&A와 Licensing 계약이 연달아 이뤄지면서 크게 주목을 받았고, 항암제 분야의 글로벌 메이저들의 추가투자 가능성이 매우 높다. 현재 전 세계적으로 이뮨온시아를 포함한 9개 기업에서 임상단계 개발을 진행 중이고, 이 중 M&A와 기술이전을 통해 파트너링이 완료된 3개사를 제외하면, 당사를 포함한 6개 회사가 'Next Big Deal'의 주인공이 될 가능성이 높다.
비임상에서 보여준 우수한 Safety/PK 프로파일을 임상에서 검증하게 되는 올해 말부터 글로벌 기술이전 기회가 본격화될 것으로 예상하고 있고, 병용 1b상을 통해 일부 암종에서의 POC데이터를 확보하게 되는 2024년에는 더욱 높은 가치로 글로벌 기술이전 기회가 있을 것으로 전망된다.
|
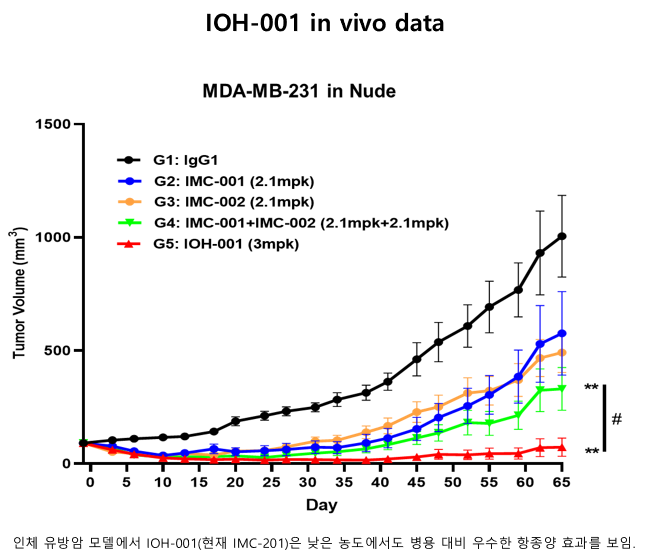
지난 4월 AACR에서 뜨거운 관심을 받았던 IMC-201(IOH-001)은 PD-L1 및 CD47 타깃의 이중항체로, 선천면역 (대식세포의 암세포 포식)과 후천면역(T세포의 암세포 살상)을 동시에 활성화하는 기전을 가졌다. 내년 하반기 IND 신청 및 승인을 목표로 세포주개발 및 공정개발 등 전임상 개발에 매진하고 있다.
이 외에도 LAG-3 단클론 항체(IMC-003)가 전임상 단계까지 개발됐고, 유한양행과 공동개발 중인 이중항체(IOH-003)와 레고켐바이오사이언스와 공동개발 중인 AIC(면역조절항체 결합체, IOH-004)가 올해 중으로 Lead 단계에 진입할 예정이다.
Q. 이뮨온시아의 비전과 마지막으로 전하고 싶은 말씀 부탁드린다.
전 세계 암환자에게 안전하고 효과적인 새로운 면역치료제를 제공하는 것을 최우선으로 하고 있다. 면역항암제 개발에 성공해, 국내 최고의 면역항암제 개발 선도기업이 될 것이며, 이를 통해 암환자들에게 혜택을 주고, 국내 면역항암제 연구 활성화와 국가재정에도 기여할 수 있는 기업이 되도록 최선을 다할 것이다.
전체댓글 0개
등록된 댓글이 없습니다.











