"품질은 시험으로 만들어지는 것이 아니라,설계와 공정 과정에서 내재화 돼야"
"품질 보증-데이터 완전성, 4차 산업혁명 시대 스마트 팩토리 진화 근본 토대"


|
국내 제약 산업 현장에서 Data Integrity(데이터 완전성, 이하 DI)는 이제 선택이 아닌 필수적인 품질 전략으로 자리 잡았다. 많은 제약 회사가 DI 전담 조직을 구성하고 ALCOA+ 원칙을 사내 곳곳에 게시하며 임직원의 인식 변화를 꾀하고 있는 점은 국내 GMP 관리 수준이 글로벌 표준에 한층 더 가까워졌음을 시사한다.
그러나 현장에서는 여전히 DI를 규제 대응을 위한 '문서화 작업’으로만 국한하여 생각할 수 있고 이를 체질화하는 것에 대해서는 어렵게 생각할 수 있다.
진정한 의미의 DI는 품질 시험서뿐만 아니라, 원료의 투입부터 타정, 코팅에 이루는 제조 공정 전반의 데이터가 얼마나 투명하고 완결성 있게 관리되느냐에 달려 있다. 이에 본 기고문에서는 추상적인 개념을 좀 더 나아가 타정 프로세스를 예를 들어 실무적이고 공학적인 관점에서 DI의 작동 방식을 이해해 보고자 한다.
설계와 공정을 통한 품질의 내재화
전통적인 제약 산업에서 품질 보증(QA) 방법은 오랜 기간 품질 검사 결과를 기반으로 해왔다. 제조 후 혹은 제조 중(가능한 경우에 한해) 무작위로 샘플링하여 검사하는 ‘시험을 통한 품질(Quality by Testing, 이하 QbT)’ 방식이 지배적이었기 때문이다.
하지만 의약품 제조 공정이 복잡해지고 규제 기관의 요구 수준이 과학화되면서, 이러한 사후 검증 모델은 더 이상 완벽해야 하는 의약품의 품질을 보증하기에는 부족하다는 한계에 직면했다.
“시험에 합격했다”는 것은 단지 추출된 샘플이 합격했다는 뜻일 뿐, 전체 제품의 균질성을 100% 보증하지 못한다. 파괴 검사가 일반적인 제약 산업의 특성상 전수 검사는 불가능하기 때문에, QbT는 태생적으로 통계적 불확실성을 내포한다. 이제 제약 품질 보증의 패러다임은 달라졌다.
“품질은 시험으로 만들어지는 것이 아니라, 설계와 공정 과정에서 내재화(Built-in)되어야 한다는 것이다.” (Quality is not tested into products; it should be built-in)
QBD와 PAT: 새로운 품질 패러다임
이러한 패러다임의 변화 속에서 등장한 QbD(Quality by Design, 설계 기반 품질)와 PAT(Process Analytical Technology, 공정 분석 기술)는 품질 관리의 화두를 '사후 검증'에서 '실시간 공정 제어(In-process Control)'로 완전히 그 중요성의 무게를 이동시켰다. 이제 품질 보증은 물리적 샘플을 파괴하여 단편적인 수치를 얻는 방식에서 벗어나, 공정의 전 흐름을 고해상도로 기록한 '디지털 증거'를 통해 품질을 입증하는 방식으로 발전했다.
예를 들어, 내용고형제 제조의 핵심인 타정 공정에서 DI는 이런 식으로 작동할 것이다. 타정기 운영중 센서 시스템에 의해 추출되는 Main Compression Force(본압), Pre-compression Force(예압), 그리고 Turret Speed(터렛 회전 속도)와 같은 데이터는 단순한 수치의 나열이 아니다. 이는 밀리초(ms) 단위로 기록되는 Time-series Data(시계열 데이터)로서, 정제의 Hardness(경도), Friability(마모도), 나아가 Dissolution Profile(용출 양상)과 긴밀한 상관관계를 갖는다.
만약 PAT 시스템이 장착된 타정장비라면, 이 시계열 데이터를 통해 별도의 테스트 없이도 해당 전체 로트(Lot)의 품질 균일성을 통계적이며 실시간으로 확인하는 것이 가능해 진다.
이런 시스템에서 만약 데이터가 의도적으로 조작되거나, 시스템 오류로 누락되어 실제 공정의 변동을 반영하지 못한다면 이는 상상하기 어려운 상황이 될 것이다. 잘못된 데이터를 근거로 한 출하 승인은 단순한 절차적 오류를 넘어, 환자의 생명과 안전을 위협하는 치명적인 품질 사고로 이어질 수 있다.
결국 ALCOA+(Attributable, Legible, Contemporaneous, Original, Accurate 등) 원칙으로 대변되는 데이터 무결성 확보 없이는 그 어떤 최첨단 스마트 팩토리나 최신 장비도 '품질'이라는 이름의 신뢰를 담보할 수 없게 된다. 이제 제약 업계는 "데이터가 곧 제품(Data is the Product)"이라는 엄중한 인식 아래, 데이터의 생(Generation)부터 보관(Retention), 폐기(Destruction)에 이르는 **Data Lifecycle(데이터 전 생애 주기)**를 엄격하고 투명하게 통제해야만 한다.
정밀 DAQ에서 SQL 보안까지: 하드웨어와 소프트웨어가 결합된 DI 시스템
특히 고형제 생산의 핵심인 타정기(Tablet Press)에서 이러한 요구 사항은 더욱 구체화된다. 최신의 타정기는 단순한 생산 장비가 아니라, 무결한 데이터를 생산하는 하나의 ‘정보 시스템’으로 기능하고 있다.
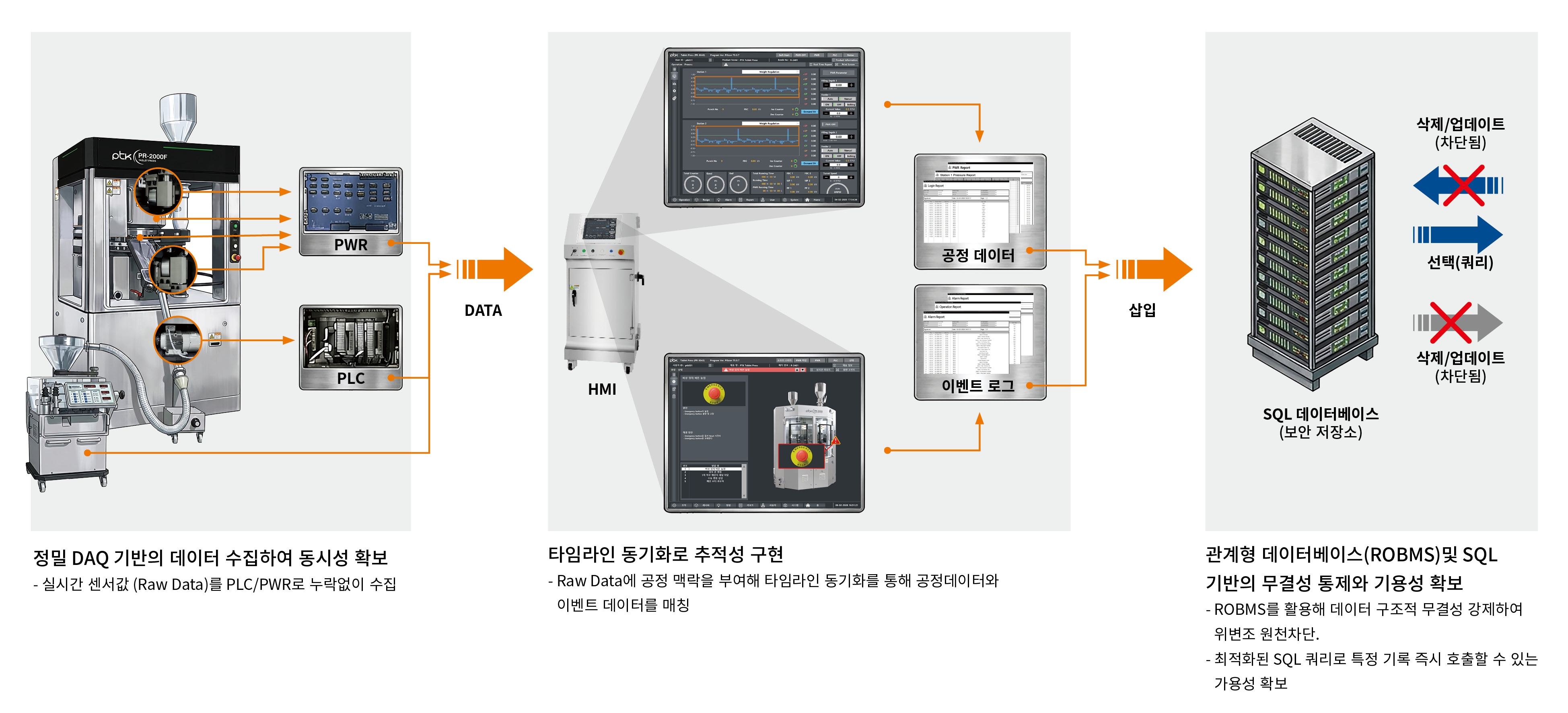
진정한 데이터 완전성은 단순히 소프트웨어 하나를 설치한다고 달성되지 않는다. 이는 ① 정밀한 데이터 수집(Acquisition), ② 시계열 동기화(TimelineSynchronization), ③ SQL 기반 관리(Management)라는 세 가지 데이터 관리 시스템이 유기적으로 결합될 때 비로소 완성된다.
첫째, 하드웨어 레벨에서의 ‘정밀한 데이터 수집(DAQ)’이다. 타정 공정의 메인 압력은 마이크로초(µs) 단위로 급변한다. 센서와 PLC는 작업자의 개입이나 필터링 없이 기계가 생성한 원본 신호(Raw Data)를 고해상도 샘플링 레이트로 즉각 포착해야 한다. 최초의 신호 포착 단계에서 누락이 발생하면 이후의 모든 데이터 관리는 의미 없는 것이 되기 때문이다.
둘째, 맥락(Context)을 부여하는 ‘타임라인 동기화’다. 수집된 숫자는 그 자체로는 의미가 없다. 공정 데이터(Process Value)와 이벤트 데이터(Audit Trail)가 ‘시간’이라는 축 위에서 완벽하게 매칭되어야 한다. 특정 시점에 타정 압력이 변했다면, 동일 타임라인에 ‘작업자의 세팅 변경’이나 ‘작동 오류’ 같은 이벤트가 있었는지 확인할 수 있어야 한다. 데이터에 전후 맥락이 보존될 때, 비로소 데이터는 단순한 기록을 넘어 규제 대응적이고 과학적 효력을 갖춘 ‘증거’가 된다.
셋째, 위변조를 원천 차단하는 ‘SQL 기반 관리’다. 여전히 일부 현장에서 사용되는 파일 기반 저장은 보안에 취약하다. 반면, 관계형 데이터베이스(RDBMS)와 SQL을 활용한 시스템은 데이터의 구조적 무결성을 강제하고 수정 및 삭제를 기술적으로 방지하거나 추적 기록한다. 또한, 방대한 데이터 속에서 특정 배치의 기록을 즉시 호출하고 분석할 수 있는 가용성(Availability)은 SQL 쿼리 최적화를 통해서만 가능하다.
|
데이터와 품질, 일심동체의 트윈스
결론적으로 현대 제약 산업에서 품질 보증과 데이터 완전성은 아마존 CEO 제프 베이조스가 말했듯 분리될 수 없는 쌍둥이(Inseparable Twins)와 같은 개념이다. ‘수집(센서) → 정렬(타임라인) → 보존(SQL DB)’으로 이어지는 견고한 기술적 시스템 구조는 단순한 규제에 대한 대응 수준 그 이상이다. 이는 과학적 근거에 기반한 배치 출하를 가능케 하고, 나아가 4차 산업혁명 시대의 스마트 팩토리로 진화하기 위한 근본적인 토대가 된다.
데이터는 거짓말을 하지 않는다. 단, 그것이 완벽하게 수집되고, 올바르게 정렬되며, 안전하게 관리될 때에만 그렇다. 이제 우리 제약 산업은 물리적 제품의 생산 속도를 넘어, 데이터의 완전성을 내재화(Built-in)할 능력에 집중해야 할 때다
-
01 "K-제약바이오, 왜 아직 ‘블록버스터 신약’ ... -
02 "오가노이드 글로벌 생태계, 한국에 모인다"... -
03 파인트리테라퓨틱스, 아스트라제네카와 EGFR... -
04 셀트리온, 유럽 EMA에 ‘허쥬마SC’ 제형 추가... -
05 K-오가노이드 컨소시엄, 2026년 정기총회 개... -
06 한미사이언스, 1분기 경영 실적 발표… 전년... -
07 에스티젠바이오, ‘비티젠’으로 사명 변경… ... -
08 한미약품, 1분기 매출 3929억 달성… 원외처... -
09 셀레믹스, 147억 규모 CB 이어 43억 유증 납... -
10 휴온스엔, 바이오로제트 흡수합병…건기식 생...










