뉴스
'자누비아' 등 '시타글립틴' 성분 56품목 허가사항 변경
'스타틴 계열 약물과 복용 시 횡문근융해증' 이상반응 추가
김용주 기자 │ yjkim@yakup.com


입력 2019-12-13 06:00 수정 2019.12.13 06:59
|
한국엠에스디의 '자누비아정25mg' 등 당뇨병치료제 '시타글립틴' 성분제제의 시판후 조사결과 이상사례가 추가로 발생해 허가사항이 변경된다.
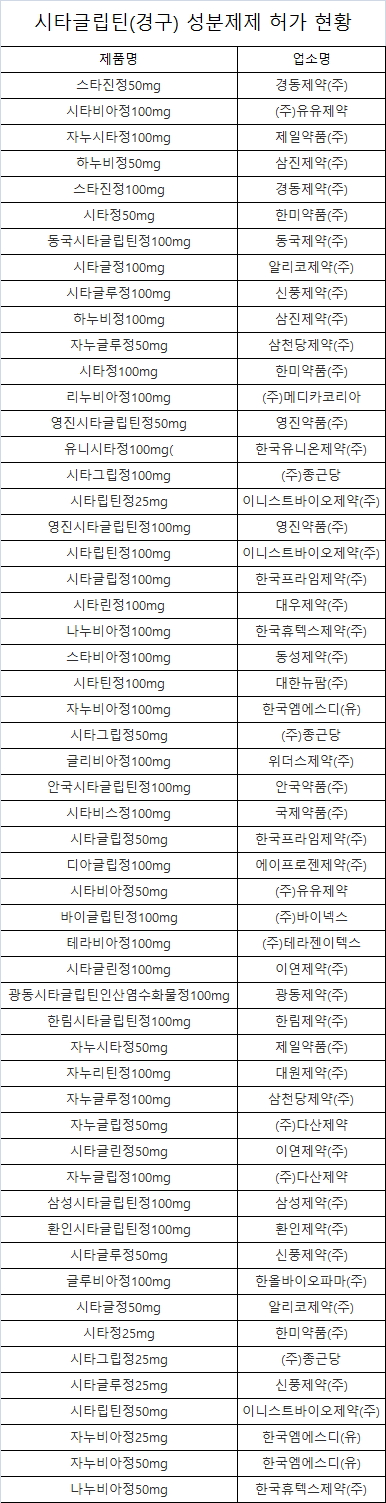
식품의약품안전처는 당뇨병치료제 '시타글립틴'성분제제(경구제)에 대한 시판 후 이상사례 보고자료 분석·평가, 중앙약사심의위원회 자문 결과 등을 국내에서 허가받은 34개사 56품목의 허가사항을 12월 30일자로 변경한다고 밝혔다.
허가사항중 이상반응항에 '시판 후 사용 중에 스타틴 계열 약물과 복용 시 횡문근융해증이 보고됐다(국내 실마리정보 분석·평가 결과)'는 내용이 추가된다.
시타글립틴 성분제제의 대표품목은 한국엔에스디의 '자누비아정25mg' '자누비아정50mg' 등이다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 석정호 대표 "우울증 조기진단,자살위험 낮... -
02 소비자 기호 맞춘 제형 다변화…판피린 ‘국민... -
03 학회 모멘텀·약가 압박 교차…제약바이오 '엇... -
04 미국, 식수 위협물질 우선순위 의약품 최초 ... -
05 흥아기연 “친환경·초고속 융합 라인, 제약포... -
06 미국, 특허의약품 100% 관세 도입…글로벌 제... -
07 베링거, ADC·TCE 중심 R&D 확대…차세대 플랫... -
08 사후 인간 뇌로 여는 CNS 신약개발…“유전자 ... -
09 [스페셜리포트] 인벤테라, 혁신 MRI 조영제 ... -
10 삼원약품 창립 52주년 “2026년, 지역 최고 ...











