뉴스
바이오솔루션, 자가연골 세포치료제 조건부 품목허가 신청 완료
무릎연골재생용 치료제 '카티라이프' 2상 임상시험 식약처 신청
이권구 기자 │ kwon9@yakup.com


입력 2018-05-16 11:16 수정 2018.05.16 11:26
|
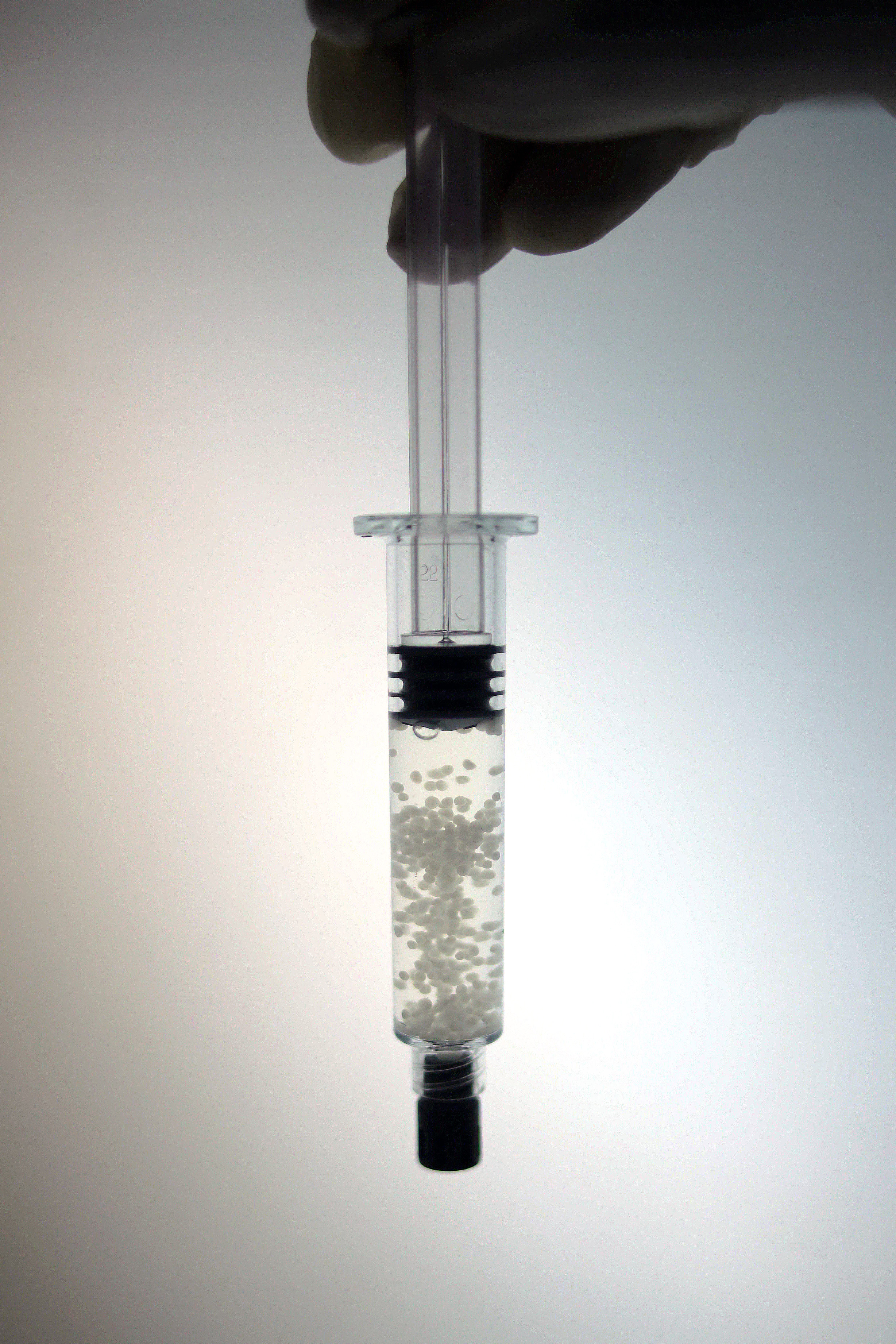
줄기세포 전문기업 바이오솔루션(대표 윤정현, 이정선)은 자가연골세포치료제 '카티라이프'의 조건부 의약품품목허가 식약처 신청접수가 완료됐다고 16일 밝혔다.
바이오솔루션에 따르면 무릎연골재생용 치료제인 카티라이프에 대해 2017년 2월 2상 임상시험을 완료하고 조건부 품목허가를 신청하기 위해 식약처와 사전검토절차를 진행해왔으며 최근 사전검토절차를 완료하고 정식으로 의약품품목허가를 신청, 접수를 완료했다.
조건부 품목허가는 임상 2상 자료를 바탕으로 의약품 시판을 허가하는 제도로 식약처는 생명을 위협하거나 중증 비가역적 질환 환자에게 치료기회를 제공하기 위해 안전성이 확인되고 치료효과가 탐색된 세포치료제에 대해조건부 허가대상을 확대하고 있다.
카티라이프는 무지지체(scaffold-free) 세포•조직공학 융합기술의 차세대 세포치료제로서 관절연골조직과 동일한 특성의 작은 구슬형 세포치료제로, 2017년 의약품분야의 보건신기술(NET)으로 선정됐다.
회사 관계자는 “ 카티라이프는 환자 연령에 관계없이 초자연골성 조직 이식으로 이식 즉시 물리적지지가 가능해 빠르고 정확한 연골재생이 가능하다” 며 “특히 작은 구슬형 연골 제조기술로 저침습성 주입식 이식으로 수술 시간 단축과 빠른 회복이 장점”이라고 설명했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 뉴로핏, 320억원 투자 유치…알츠하이머 치료... -
02 대웅제약, '펙수클루정' 적응증 추가 임상3... -
03 신테카바이오,항암-면역질환 항체 후보물질 ... -
04 다임바이오, ‘초격차 스타트업 1000+’ 선정…... -
05 중국 ‘이노벤트’, 바이오 CDMO 진출..글로벌... -
06 병원 유통업계, 대웅 유통개편 확산 경계…"... -
07 다이이찌산쿄, ADC 생체지표 발굴 AI 접목 제휴 -
08 "단일 학문 넘어 융합의 시대로"… 한국약제... -
09 메디톡스, 히알루론산 필러 ‘뉴라미스’ 2종 ... -
10 시지메드텍, 성남 인체조직은행 인수… ECM ...











