
제약바이오업체들의 스마트공장 구축을 위해 식약처가 시험제, 경피흡수제, 점안제 등 제형별 QbD 모델을 잇따라 개발 공개할 방침이다.
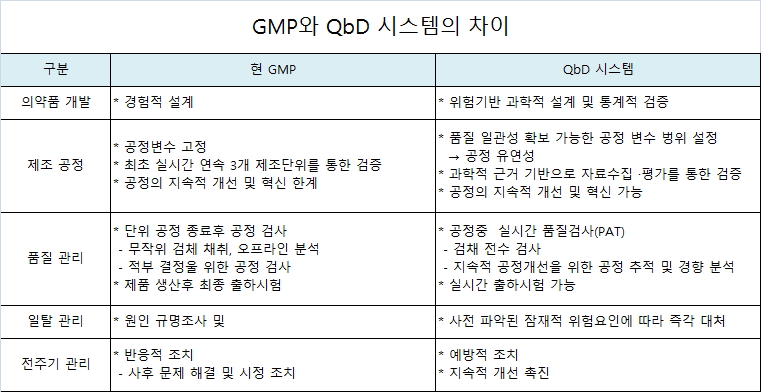
식품의약품안전처는 현재의 GMP기준을 제조와 품질관리가 이원화돼 제조공정 단계의 잠재적 위험성을 예측할 수 없어 생산 효율성 관리가 어렵다는 판단아래 의약품 품질고도화시스템(QbD, Quality by Design0 도입을 추진해오고 있다.
의약품 품질고도화시스템(QbD, Quality by Design)은 의약품 제조·품질관리의 새로운 패러다임으로, 의약품의 전주기(개발~판매중단) 사전 위험평가를 통해 실시간으로 제품특성에 맞는 최적의 품질관리를 구현하는 시스템이다.
미국, EU, 일본 등 제약 선진국은 QbD 도입해 정착 단계이고, 아세안지역도 QbD 자료를 요구하고 있는 추세이다.
|
식약처는 의약품실사상호협력기구(PIC/S) 회원국 가입(2014년 7월), 국제의약품규제조화위원회(ICH) 회원국 가입(2016년 11월)이후 QbD 개념이 도입된 국제 규제와의 동등성 확보에 나서고 있다.
지난 2015년 일반방출정제와 복합이층정제에 대해 실험실 QbD 모델을 제시한 이후, 2016년 캡슐제, 2017년 주사제에 대해 QbD 모델을 개발해 공개했다.
이중 일반방출정제와 캡슐제는 시생산 단계까지 제시한 상황이고, 식약처는 올해중 복합이증정제와 주사제에 대해 시생산을 한다는 계획이다.
또 내년에는 시럽제, 경피흡수제, 점안제 등에 대해 시험실 QbD 모델을 개발하고, 2021년부터 시생산을 가능하도록 한다는 방침이다.
특히 식약처는 제약사들의 QbD 도입을 지원하기 위해 제약사별 QbD 적용 의약품 개발을 위한 맞춤형 컨설팅, 전문인력 양성을 위한 교육을 확대한다는 계획이다.
식약쳐는 의약품 품질고도화시스템(QbD) 도입과 정착을 통해 제약·바이오 스마트공장 구축의 기반을 마련하고, 나아가 생산 효율성 향상으로 품질 경쟁력을 확보해 의약품 수출이 확대될 것으로 전망하고 있다.
-
01 바이오솔루션, 순이익 122억원 늘며 '흑자전환' -
02 한국감사협회, ‘내부감사·컴플라이언스 전문... -
03 GC녹십자, 면역글로불린 내 ‘혈전 유발 불순... -
04 미국 제약협회, 의약품 관세 도입 반대입장 ... -
05 노보 “릴리 ‘파운다요’보다 ‘위고비’ 정제가... -
06 한미약품, 미국암연구학회서 국내 최다 연구... -
07 [약업 분석] 코오롱생명과학, 적자 늪 벗어... -
08 유전자교정협의회 "한국 규제, 글로벌과 불... -
09 롯데바이오로직스, 일본 제약사와 항암 항체... -
10 SK바이오팜, AACR서 방사성의약품 성과 공개...











