
식약처가 제네릭 의약품 품질검사 연구결과 대상 품목 모두 적정품질을 유지하고 있다고 밝혔으나, 실제 의약품 동등성 시험결과에 대한 품질 유효성 신뢰도에 의문이 제기되고 있다.
식품의약품안전처는 10일 국내 유통 의약품 품질연구 결과(이하 '제네릭 품질검사')15개 품목 중 6개 품목은 의약품 동등성 시험 범위 수준을 벗어났다.
식약처의 발표대로 법적 품질수준(80%~125%)에는 이상이 없다. 그러나 상세 시험내용을 살펴보면 본래 의약품동등성시험기준 중 생동성 시험기준을 벗어난 제품이 2개, 비교용출 시험기준을 벗어난 제품도 6개다.
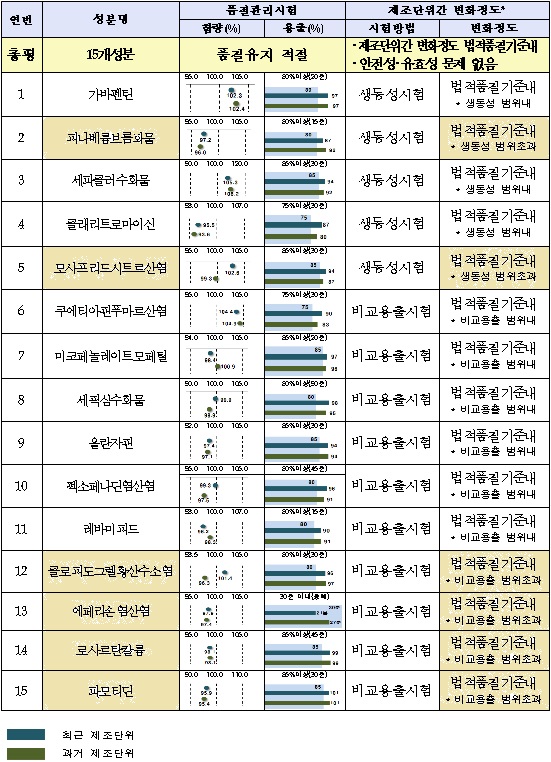
|
비교용출 시험대상 품목 중에서는 △한림제약의 피도빅스정(성분명 클로피도그렐황산수소염) △한국유니온제약 에손정(성분명 에페리손염산염) △씨트리 로자틴정(성분명 로사르탄칼륨) △셀트리유온제약의 셀트리온파모티딘정(성분명 파모티딘)은 비교용출 범위를 초과했다.
시험범위를 초과했다는 것은 법적 품질수준(80%~125%)을 벗어났다고 해석할 수 있기에 문제가 될 수 있다.
생동성 시험에서 생동성 범위를 초과했다는 것은 AUC(시간에 따른 혈중 약물농도의 합)과 Cmax(혈중최고약물농도)를 벗어났다는 의미이기 때문이다.
식약처는 "제네릭 품질검사 대상 품목들이 생동성 범위는 초과했으나, 품질 적정범위 내에는 포함되어 약제의 안전성과 유효성에는 문제가 없다"며 "시험 결과는 전세계적으로 유례없이 제조단위간 시험을 시행해 엄격히 진행됐으며, 중앙약사심의위원회의 최종검토를 거친 결과다"고 설명했다."는 입장을 밝혔다.
일부 제품에서 제조단위 간 품질이 차이가 있었으나, 모든 제조단위가 제품별 품질기준에 적합하고, 품질기준에 적합한 각각의 제조단위간 품질 변화정도는 치료효과나 부작용에 영향을 미치는 수준이 아니라는 것.
오리지널과 비동등한 제네릭이나 안전에는 문제가 없다는게 식약처의 결론이나, 제조단위 제품 간 생동성 시험에서 시험 범위 기준을 벗어난 제품들이 적절한 품질을 유지하고 있다고 보기에는 의문이 제기될 수 있다.
이에 시험대상 각 품목별 생동성 시험, 비교용출 시험 결과 공개를 요청했으나 식약처는 이를 거부하고 있는 상태다.
'유통 의약품 시험 검증'이라는 이름으로 실시된 이번 사업은 국산 제네릭의 '의약품 동등성 검증'을 위해 진행된 사업이다. 그러나 식약처의 시험결과 발표는 의약품의 '동등성'이 아닌 '품질'에 대한 분석만 포함되어 있어 제네릭 의약품의 동등성 논란을 불러 일으킬 전망이다.
-
01 오스코텍,유한양행 기술이전 마일스톤 분배... -
02 인벤테라, 나노-MRI 조영제 신약 'INV-002' ... -
03 라메디텍, 인체조직은행 식약처 허가...ECM ... -
04 한미사이언스, ‘랩스커버리’ 등 한미 핵심 ... -
05 유한양행, ‘레이저티닙(렉라자)’ 유럽 상업... -
06 네오메디칼제약, 약국 전용 프리미엄 치약 ... -
07 리가켐바이오, CLDN18.2 ADC 글로벌 임상 본... -
08 삼아제약, 1분기 수익성 둔화…재무안정성은 ... -
09 큐로셀 김건수 대표 “국내 첫 CAR-T 림카토,... -
10 고용량 ‘위고비’ 체지방 위주 체중감소 28% ...










