뉴스
식약처, 방사성의약품 등 16개 의약품 GMP신설
PIC/S 후속조치…의약품 제조 및 품질관리 규정 제정
신은진 기자 │ ejshin@yakup.com


입력 2015-06-22 10:15 수정 2015.06.22 13:31
|
PIC/S 가입에 따라 오는 7월부터 방사성의약품 등 16개 의약품에 대한 GMP가 신설된다.
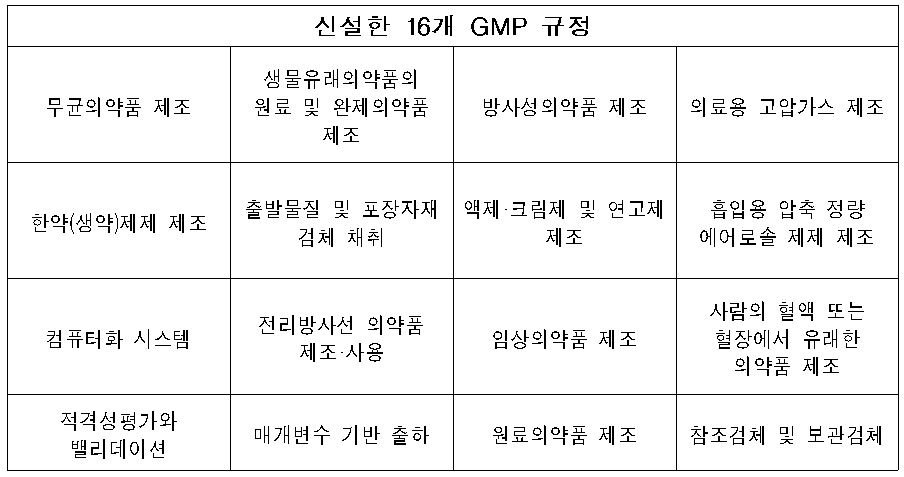
식품의약품안전처(처장 김승희)는 무균의약품, 방사성의약품 등 16개 제조 및 품질관리 기준(GMP) 규정을 신설하는 것을 주요 내용으로 하는 '의약품 제조 및 품질관리에 관한 규정'을 올해 7월부터 시행한다고 22일 밝혔다.
이번 제정고시는 ‘의약품실사상호협력기구(PIC/S)’ 가입에 따라 지난 1월 행정예고를 거쳐 6월 17일 제정됐다.
주요 내용은 PIC/S GMP 규정과 조화하여 무균의약품, 방사성의약품 등 16개 의약품 GMP의 신설 및 의무화이다.
또한 GMP 평가 후 발급하는 ‘GMP 적합판정서’의 유효기간을 3년으로 정했으며, 품목별 GMP 심사대상에 무균원료의약품, 복막투석제, 관류제, 점안제 및 안연고제를 포함시켰다.
식약처는 "이번 제정고시를 통해 PIC/S 가입에 따른 국제 조화된 제조 및 품질 관리 시스템 구축과 동시에 국내 제조 의약품의 상향된 GMP 체계를 완비함으로써 우수한 품질의 의약품을 공급하여 국민건강을 향상시키고 글로벌 시장을 확대할 수 있는 수출경쟁력 강화에 기여할 것이다"고 말했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 복지부 1차관에 현수엽 현 보건복지부 대변... -
02 "코스닥 상장 힘 받았다" 넥스아이, 500억원... -
03 차백신연구소, 김병록 경영지배인 선임 -
04 쿼드메디슨,한림제약과 마이크로니들 기반 ... -
05 “AI로 반복 심사 줄인다”… 식약처 화장품 안... -
06 아이엠비디엑스 "액체생검, 암 전주기 커버... -
07 셀리드, 항암면역치료백신에 적용된 NK세포 ... -
08 한국병원약사회 전문약사 수련 확대…현장은 ... -
09 제이브이엠, 중국 쑤저우 생산기지 준공…글... -
10 KSMO 박준오 이사장 “종양내과, 항암치료 넘...










