
|
재생의학 스타트업 오가노이드사이언스(대표 유종만)가 국내 최초로 미국 식품의약국(FDA)의 ‘혁신적 과학·기술 접근(ISTAND, Innovative Science and Technology Approaches for New Drugs) 파일럿 프로그램’에 오가노이드 기반 약물 흡수도 평가법을 공식 제출했다고 16일 밝혔다.
ISTAND는 기존 규제 경로가 없는 새로운 약물개발 도구(DDT, Drug Development Tool)를 FDA가 단계적으로 검증해 공인 시험법으로 발전시키는 제도다. 2020년 출범 이후 인체 장기칩·AI 기반 디지털헬스 기술 등이 채택되며 동물대체시험의 핵심 통로로 주목받고 있다.
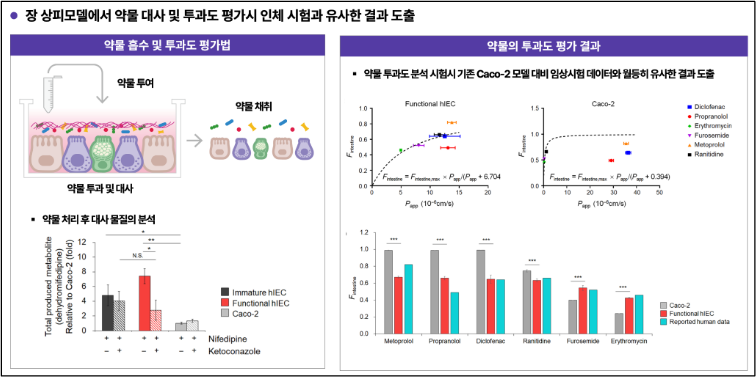
이번에 제출된 후보 기술은 한국생명공학연구원(KRIBB) 손미영 국가아젠다연구소장 연구팀이 개발한 ‘인체 장 상피 오가노이드 모델’을 이용해 경구 약물의 흡수율을 예측하는 시험법이다. 오가노이드사이언스는 2023년에 해당 기술을 이전받아 표준화 프로세스를 구축했고 상용화에 성공해 서비스를 제공 중이다. 현재는 신약 후보의 경구 흡수성을 확인하기 위해 비글견에 투여해 혈중 농도를 측정하지만, 새 모델이 ISTAND 승인을 받아 공인 시험법으로 등재되면 비글견 실험을 대폭 줄일 수 있을 전망이다.
ISTAND 프로세스는 ‘접수 → 과학자문 → 프로토콜 동의 → 예비검증 → 완전 검증’의 5단계로 진행된다. 이번 제출은 1단계 접수를 마친 상태이며 FDA는 60일 이내 수용 여부를 통보한다. 수용 시 FDA 과학자문단이 시험 디자인과 통계 분석 계획을 코칭하고, 필요한 경우 미국 내 전임상 센터와의 연계 시험도 지원한다.
ISTAND 프로젝트를 총괄하는 오가노이드사이언스 황동연 CSO는 “국내 기술이 FDA 제도적 관문을 통과한다는 상징성이 크다”며 “사람 장기에 더 가까운 데이터를 확보해 글로벌 임상 성공률을 높일 것”이라고 말했다.
한국생명공학연구원 손미영 소장도 “장기 오가노이드가 in vivo 데이터를 대체할 수 있다는 사실을 국제적으로 입증할 기회”라며 “향후 주요 장기 오가노이드를 활용한 다장기 플랫폼으로 확장할 것”이라고 강조했다.
글로벌 경구제 파이프라인은 연간 1만 건이 넘지만, 흡수율 예측 불일치로 30 % 이상이 IND 단계에서 탈락한다. 인체 상피 오가노이드는 사람 특이적 약물 운반체와 대사효소 발현을 보존해 예측도가 높다. EMA와 PMDA도 3R(Replace·Reduce·Refine) 정책을 강화하는 가운데, ISTAND 진입은 한국 기업이 동물대체시험 국제 표준 주도권을 확보하는 계기가 될 전망이다.
전문가들은 “ISTAND 채택 여부와 무관하게 해당 모델이 민감도와 재현성이 입증되면 제약사가 초기 독성·제제 최적화를 위해 자발적으로 도입할 것”이라며 “이는 전임상 단계에서 평균 6개월의 연구 기간과 수십 마리 동물 사용을 단축해 연간 1억 달러 이상 비용 절감 효과를 가져올 수 있다”고 분석한다.
오가노이드사이언스는 2026년까지 검증 데이터를 확보해 2027년 ‘완전 검증’ 달성을 목표로 한다. 목표 달성 시 시험법은 FDA 및 ICH 가이드라인에 통합돼 모든 제약사가 이용할 수 있는 공용 도구가 된다. 회사는 세포주 공급, 분석 플랫폼, 데이터 관리 소프트웨어를 패키지화해 연 매출 300억 원 이상 새 시장을 창출할 계획이다.
FDA의 수용 결정은 이르면 8월 중순 발표될 예정이다. ISTAND 지원을 받는 글로벌 최초 오가노이드 기반 시험법으로 채택되어 오가노이드사이언스가 ‘비글 없는 경구 약물 시험’ 시대를 열 수 있을지 귀추가 주목된다.
-
01 대한약사회 “정부는 한약사 문제 즉시 해결... -
02 바이오솔루션,연골세포치료제 '카티로이드' ... -
03 동아쏘시오홀딩스, 바이오시밀러 상반기 매... -
04 유한클로락스,창립 50주년 새 기업 로고 공개 -
05 GC녹십자,텍사스주 혈장센터 개소..내년 상... -
06 HLB, HLB사이언스 흡수합병... 패혈증 신약 ... -
07 부광약품 자회사 콘테라파마, ‘CP-012’ 1b상... -
08 바이오솔루션, 흥케이병원과 연골재생치료 ‘... -
09 명인제약, 공모가 상단 58000원 확정…의무보... -
10 이엔셀, 세계 최대 세포유전자치료제 컨퍼런...











