뉴스
‘아두카누맙’ 첫 권고안 발표…‘ARIA’ 모니터링에 MRI 필수
2021 알츠하이머 국제회의서 공개‥ 임상·약물개발 전문가 참여해 의료진 위한 지침 만들어
김상은 기자 │ kims@yakup.com


입력 2021-07-29 06:00 수정 2021.07.30 11:06
알츠하이머 초기 경증 질환의 치료 목적을 위한 아두카누맙(Aducanumab(상품명: 에두헬름;Aduhelm))에 대한 첫 번째 권고안이 발표됐다.
이번 권고안은 아두카누맙이 사용되고 있는 미국 내의 임상현장에서 적용될 예정이다.
현재 네덜란드 암스테르담에서 개최되고 있는 2021년 알츠하이머협회 국제회의(AAIC)에서는 ‘아두카누맙: 적절한 사용 권장사항’을 주제로 전문가들이 모여 발표하는 자리가 마련됐다.
지난 27일(현지시간)에 발표된 이 권고안은 아두카누맙의 임상시험 정보, 업데이트된 FDA 처방 정보를 바탕으로 알츠하이머 연구, 임상 실험 및 약물 개발 경험이 있는 전문가들의 논의를 통해 만들어졌다.
권고안 지필에는 UCLA 신경학 교수인 제프리 커밍스(Jeffrey Cummings) 박사와, 로드 아일랜드의 버틀러 병원의 신경학과 책임자 스테픈 살로웨이(Stephen Salloway) 박사 등이 참여했다.
Jeffrey Commings 박사는 “아두카누맙은 전례 없는 치료제라는 점에서 약물을 사용하는 의료진에게 효과적이고 안전한 사용을 위한 지침을 제공하는 것이 목표”라고 밝혔다.
이 권고안은 처방된 정보와 실제 임상 현장에서 발생하는 간극을 메우고자 의약품의 적절한 환자와 복용량을 식별하고, 부작용에 대한 모니터링 및 예상 부작용, 위험에 대해 정확히 전달하는 의사소통에 대한 방향을 담았다.
|
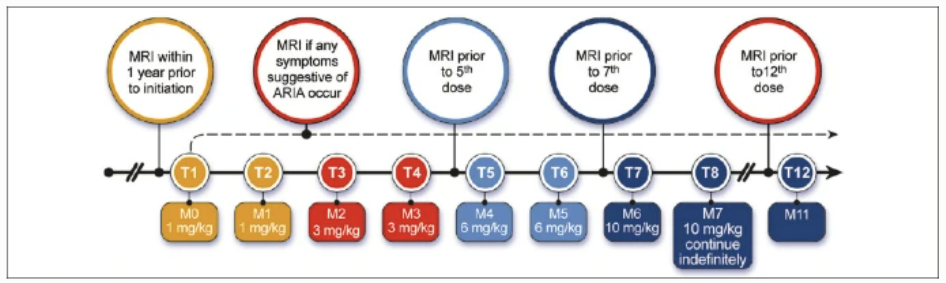
권고안에는 ▲처방 대상은 연구된 모집단(경증 치매환자)으로 제한 ▲가장 높은 용량으로 적정 ▲자기공명영상촬영은 약물 복용 전후로 시행 ▲환자의 개인 보고 중심의 측정 방식이란 점에서 명확한 소통의 필요성이 포함됐다. 추가적으로 아밀로이드 관련 영상 이상(ARIA)이 의심 될 경우 치료를 중단시켜야 한다는 권고사항이나 본 약물에 제외되어야 할 환자군에 대한 설명도 포함됐다.
하지만 이번 권고안에 이어 아두카누맙에 대한 장기적인 사용에는 공동의 합의에 바탕한 계획이 필요할 것으로 보인다.
권고안이 발표된 당일 ‘알츠하이머병 예방 저널’에서는 임상현장에 아두카누맙이 도입되면서 알츠하이머 신경영상계획(ADNI)에도 혼선이 빚어질 것이라는 예측을 내놨다.
현재 아두카누맙의 부작용으로는 대표적으로 뇌출혈이나 ARIA와 같은 심각한 부작용도 잠재적으로 나타나고 있는데 이를 위해서는 MRI를 통한 지속적인 감시가 필요하기 때문이다.
하지만 ADNI에 대한 모든 의료자원이 아두카누맙 사용에 따른 뇌영상 촬영에 집중되다보면 ADNI와 같은 관찰 연구와 무작위 임상실험을 포함한 모든 종류의 알츠하이머 질환(AD) 임상 연구를 더욱 어렵게 만들 것이라는 점이다.
이날 권고안에서도 “아두카누맙의 적절한 사용을 위한 기반시설을 구축하려면 시간과 자원, 그리고 계획을 수립해야 할 것”이라고 지적했다.
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 대한약사회 권영희 집행부 1년…약준모 회원 ... -
02 인트론바이오, 박테리오파지 ‘드롭인’ 제형 ... -
03 보령, 국내 최초로 청소년 그림 달 표면 보... -
04 GC녹십자, 미국 라레도 혈장센터 FDA 허가 ... -
05 카나프테라퓨틱스, AACR 2026서 이중항체 항... -
06 SK바이오사이언스, ‘2026 스카이 비전 심포... -
07 이엔셀, MSAT에 AI 기술 더해 CDMO 역량 고도화 -
08 “주사에서 알약으로”…K-바이오, '포스트 릴... -
09 동화약품, 신용재 중선파마 호치민 지사장 선임 -
10 아델, 490억 규모 Pre-IPO 유치 …코스닥 상...











