세포주·업스트림·다운스트림·분석 전주기 통합 설계 필요
바이오의약공방, HCP 관리 전략 콜로키움 성료

|

|
바이오의약품 ‘잔류 숙주세포 단백질(Host Cell Protein, 이하 HCP)’ 관리는 더 이상 총량 저감 문제가 아니다. 임상 후기나 상업화 단계에서 드러나는 핵심 품질 리스크가 특정 HCP에서 비롯되기 때문이다. CMC 전략 중심도 총 HCP 감소에서 ‘고위험 HCP 통제’로 이동하고 있다.
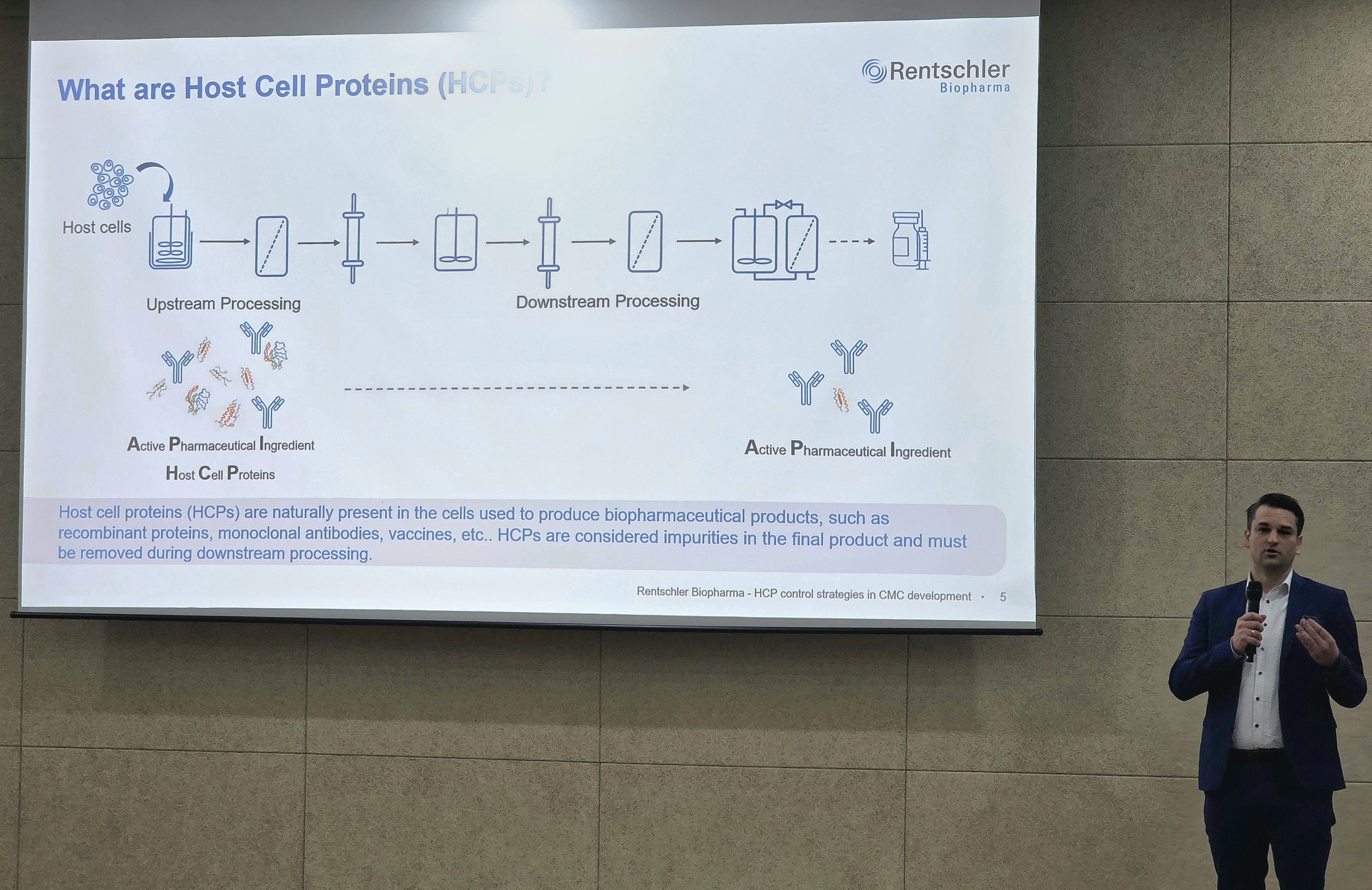
렌슬러 바이오파마(Rentschler Biopharma) 아시아 사업개발 총괄(Head of Business Development Asia) 콘스탄틴 바그뉵 박사(Dr. Konstantin Bagnjuk)는 10일 바이오의약공방이 인천 연세대학교 송도 국제캠퍼스에서 개최한 ‘Host Cell Proteins(HCPs) 분석과 관리 방법’ 콜로키움에 연사로 참석, ‘리스크에서 통제로: CMC 개발에서의 숙주세포 단백질 관리’를 주제로 발표했다.
렌슬러 바이오파마는 1927년 독일에서 설립, 약 100년의 역사를 가진 글로벌 바이오의약품 위탁개발생산(CDMO) 기업이다. 까다로운 항체 및 다중특이항체나 재조합 단백질 등 개발과 정제 난도가 높은 바이오의약품 공정 개발(CMC)에 특화된 기술력을 보유한 기업으로 널리 알려져 있다.
그는 HCP를 세포주 개발부터 업스트림 공정(USP), 다운스트림 공정(DSP), 분석 전반을 관통하는 핵심 품질관리 항목이라고 강조했다. 세포주 설계와 공정 조건, 분석 전략 등 초기 단계의 선택이 최종 HCP 관리 수준을 좌우한다고도 설명했다.
바그뉵 박사는 “총 HCP ppm이 낮다고 해서 리스크가 사라졌다고 볼 수는 없다”면서 “실제 품질 이슈는 소수의 고위험 HCP가 좌우하는 경우가 많고, 그 정체를 밝혀내지 못하면 안정성 문제를 뒤늦게 맞게 된다”고 지적했다.
이번 세미나 기획과 좌장을 맡은 송도컨설팅그룹 황후상 박사는 “국내 바이오 기업들이 여전히 HCP를 총량 중심의 불순물 관리 수준으로 접근하는 경향이 있지만, 글로벌 규제 환경은 개별 HCP의 기능적 활성까지 평가하는 방향으로 강화되고 있다”고 말했다.
이어 황 박사는 “이제는 어떤 HCP가 남아 있고 그것이 제품 품질에 미치는 영향을 설명할 수 있는 역량을 갖춰야 할 때”라며 “글로벌 진출을 위해서는 세포주부터 공정, 분석까지 HCP 관리 체계를 통합적으로 설계하고, 관리 수준을 근본적으로 끌어올려야 한다”고 강조했다.
문제는 총량 아닌 고위험 HCP
HCP는 CHO 세포 등 발현 숙주에서 유래하는 단백질로, 세포 기반 발현 시스템을 사용하는 바이오의약품 제조 과정에서 공정 불순물로 관리된다. 이들 단백질은 응집, 산화, 절단·분해를 유도하거나 면역원성 및 사이토카인 방출과 연관이 있다.
실제 리스크는 전체 HCP 양이 아니라 특정 고위험 HCP에서 발생하는 경우가 많다. 대표적으로 프로테아제(protease), 리파아제·에스터레이스(lipase·esterase), 면역원성 우려 HCP, 최종 목적 단백질 등에 달라붙어 함께 정제되는 이른바 '히치하이킹 HCP(Hitchhiking HCP)'가 꼽힌다.
바그뉵 박사 후기 개발 단계 프로젝트에서 발생한 HCP 관련 사례를 제시했다. 해당 프로젝트에서는 장기 안정성 시험 이후 완제의약품에서 입자가 발생했으며, 분석 결과 입자 내 지방산 함량 증가가 확인됐다.
원인 분석 결과, 제형 안정화제인 폴리솔베이트 20(Polysorbate 20)을 분해하는 리파아제 활성(Lipase activity)을 가진 HCP가 원인이었다. 특히 총 HCP 수치와 리파아제 활성 간에는 직접적인 상관관계가 나타나지 않았다.
연구팀은 총량 분석과 별도로 리파아제 활성을 정량하는 효소 활성 분석법을 구축하고, Protein A 크로마토그래피 세척 조건과 심층여과(depth filtration), 폴리싱 공정(polishing)을 단계적으로 재설계했다. 그 결과, 리파아제 활성을 유의미하게 낮추고 입자 발생을 억제하는 데 성공했다.
바그뉵 박사는 “이처럼 실제 리스크는 폴리솔베이트 20을 분해하는 리파아제처럼 특정 HCP의 기능적 활성에서 비롯되는 경우가 많고, 이러한 단백질은 총량 분석만으로는 포착되지 않는다”고 강조했다.
CMC 출발점은 세포주…초기 HCP 부하 설계가 좌우
HCP 관리 출발점은 다운스트림 공정에 국한되지 않고, 세포주 개발부터 업스트림 공정에 이르는 전 과정에서 HCP 관리 전략이 함께 설계돼야 한다.
HCP 발생과 제거를 동시에 고려한 설계가 필요하며, 특히 세포주 단계에서의 HCP 부하 설정이 전체 공정의 난이도와 품질 리스크를 좌우하는 핵심 변수로 작용한다고 바그뉵 박사는 설명했다. 특정 고위험 HCP를 노크다운(knock-down) 또는 노크아웃(knock-out)하는 접근이 가능하지만, 이는 세포 생존율과 생산성에 영향을 줄 수 있는 상충 관계를 동반한다.
업스트림 공정에서도 배지 공급 전략(feeding strategy), 전단응력(shear stress), 배양 시간, 수확 조건 등이 세포 손상과 단백질 누출에 영향을 미치며, HCP 발생 수준을 결정하는 주요 변수로 작용한다. 특히 수확 과정에서의 물리적 스트레스는 세포 손상을 유도하고, HCP가 대량으로 유입되는 주된 원인으로 지목된다.
초기 단계에서 HCP 부하를 충분히 낮추지 못하면 이후 다운스트림 공정에서 제거 부담이 급격히 증가하고 품질 리스크도 함께 확대될 수밖에 없다는 것이다.
바그뉵 박사는 “다운스트림 공정에서 HCP를 줄이는 것도 중요하지만, 세포주와 업스트림 공정 단계에서부터 불필요한 HCP 부하를 낮춰 놓지 않으면 이후 공정에서 제거 비용과 복잡성이 급격히 증가한다”고 지적했다. 이어 “HCP 관리는 정제 기술의 문제가 아니라 세포주 설계와 공정 조건을 포함한 초기 개발 전략의 문제”라고 강조했다.
HCP 제거는 단일 공정 아닌 누적 설계
다운스트림 공정은 HCP 제거가 실제로 이뤄지는 핵심 단계다. 발표에서 제시된 이중특이항체 예시 공정에서는 Protein A 크로마토그래피 단계에서 약 2-log 수준의 HCP 감소가 확인됐고, 이후 저 pH 기반 바이러스 불활화와 심층여과(depth filtration)를 거치면서 추가적인 제거가 이뤄졌다.
그러나 모든 HCP가 동일하게 제거되는 것은 아니다. 일부 HCP는 제품과 결합하거나 복합체를 형성한 상태로 공정을 통과하며, 정제 과정 전반에서 함께 이동한다. 이러한 동반 정제 HCP는 특정 공정 단계만으로는 효과적으로 제거하기 어렵다.
이에 따라 HCP 제거는 개별 공정의 제거 효율이 아니라, Protein A 크로마토그래피를 포함한 포획 단계(capture)부터 바이러스 불활화, 여과, 폴리싱 공정까지 각 단계가 어떻게 연결되고 상호작용하는지에 따라 결정된다는 분석이다.
바그뉵 박사는 “HCP 제거는 특정 공정 하나의 성능으로 설명할 수 있는 문제가 아니다”며 “각 공정 단계가 어떻게 연결되고 누적되는지를 함께 봐야 전체 공정의 통제력을 평가할 수 있다”고 강조했다.
분석 전략도 변화…ELISA에서 LC-MS로 확장
HCP 분석 전략 역시 변화하고 있다. 기존에는 ELISA 기반 총량 측정이 표준적으로 사용돼 왔지만, 이는 어떤 HCP가 존재하는지, 특히 어떤 단백질이 품질 리스크를 유발하는지까지는 확인할 수 없다는 한계가 있다.
LC-MS 기반 분석이 확대되며, 개별 HCP의 정체와 함량을 동시에 파악하는 접근이 중요해지고 있다. ELISA가 전체 HCP 수준을 관리하는 도구라면, LC-MS는 리스크를 유발하는 특정 HCP를 식별하는 분석법으로 활용되고 있다.
또한 공정 특이적(process-specific) ELISA 분석법 개발에는 약 1.5년이 소요될 수 있어, 개발 초기 단계에서 분석 전략을 함께 설계하지 않을 경우 임상 일정 지연으로 이어질 가능성도 지적됐다.
바그뉵 박사는 “초기 단계에서는 상업용 키트로 시작할 수 있지만, 후기 단계로 갈수록 공정 특이적 분석법이 사실상 요구된다”며 “이 전환을 늦게 시작하면 개발 일정 자체가 영향을 받을 수 있다”고 말했다.
‘공정 기반 입증’ 규제 요구 강화
규제 환경도 HCP 관리 전략의 정교화를 요구하는 방향으로 움직이고 있다. EMA는 HCP를 일반적으로 지속적인 관리가 필요한 단백질성 공정 불순물로 보고 있다. 단순 제거 수준이 아니라 공정 전반에서의 관리 전략과 분석법의 적절성에 대한 정당화를 요구하고 있다.
특히 바이오시밀러는 HCP를 포함한 공정 관련 불순물 관리 전략은 대조의약품(reference product)을 그대로 따르는 것이 아니라, 자사 제조 공정과 생산 경험을 기반으로 설정해야 한다는 점이 강조되는 추세다.
USP 역시 기존 ELISA 기반 총량 분석에 더해 LC-MS 등 직교적 분석 접근을 보완 전략으로 제시하며, 개별 HCP 수준에서의 정체 규명과 리스크 평가를 요구하는 흐름을 반영하고 있다.
업계에 알려진 HCP 초기 100 ppm, 후기 10 ppm 수준은 명문화된 규제 기준이라기보다 인허가 대응 과정에서 축적된 실무적 목표치에 가깝다. 절대적인 기준이라기보다는 개발 단계별 리스크 관리 수준을 가늠하는 경험적 지표로 해석해야 한다는 설명이다.
바그뉵 박사는 “HCP 관리는 이제는 수치를 낮추는 것에서, 어떤 단백질이 남아 있고 그 단백질이 바이오의약품의 품질과 안정성에 어떤 영향을 미치는지를 이해하고 통제하는 문제”라고 말했다. 이어 “바이오의약품의 CMC 경쟁력은 HCP의 위험성을 얼마나 깊이 이해하고 공정에 선제로 반영하느냐에 달려 있다”고 강조했다.
바이오의약공방 설립자인 김형순 박사는 “이번 콜로키움은 국내 바이오 기업들이 글로벌 바이오의약품 개발 기준에 부합하는 역량을 확보할 수 있도록, 현장에서 검증된 글로벌 기업 연사를 초청해 실질적인 인사이트를 공유하기 위해 마련됐다”며 “HCP 관리와 같은 핵심 품질 이슈를 개발 초기부터 반영하는 것이 글로벌 경쟁력의 출발점”이라고 말했다.

|

|

|
-
01 네오켄바이오,의료용 헴프 기반 CBD 원료의... -
02 셀트리온 '옴리클로' 맞춤 영업 성과 본격화... -
03 레이저옵텍, 유증 구주주 청약률 109.5% .. ... -
04 프로티어바이오텍, 분자접착제 기반 혁신 항... -
05 질경이,30억 원 투자 유치… "2027년 코스닥 ... -
06 100년 역사 렌슬러, 한국서 바이오 HCP 리스... -
07 상장 제약·바이오 2025년 평균 R&D비 코스피... -
08 "약국이 가격 비교 대상"…창고형 약국에 현... -
09 노바티스 구조조정 지속…뉴저지 HQ 추가 감... -
10 나노·RNA·AI 이미징… 신약 개발의 판도를 바...











