
|
지난해 FDA가 승인한 신약 55개 중 29개(23.7%)가 희귀의약품지정(Orphan Drug Designation)을 받은 것으로 나타났다. 이 중 14개(48%)는 신흥 바이오제약 기업(Emerging BioPharma)이 개발한 신약이다. 신흥 바이오제약 기업이 신약 개발 성공률을 높이는 방법으로 희귀유전 질환 타깃 전략이 제시되는 이유다.
아이큐비아(IQVIA) EMEA 사고적 리더십(EMEA Thought Leadership)팀은 최근 ‘희귀에서 기회로: 희귀질환 출시 우수성 마스터(From Orphan to Opportunity: Mastering Rare Disease Launch Excellence)’ 보고서를 통해 이같이 밝혔다.
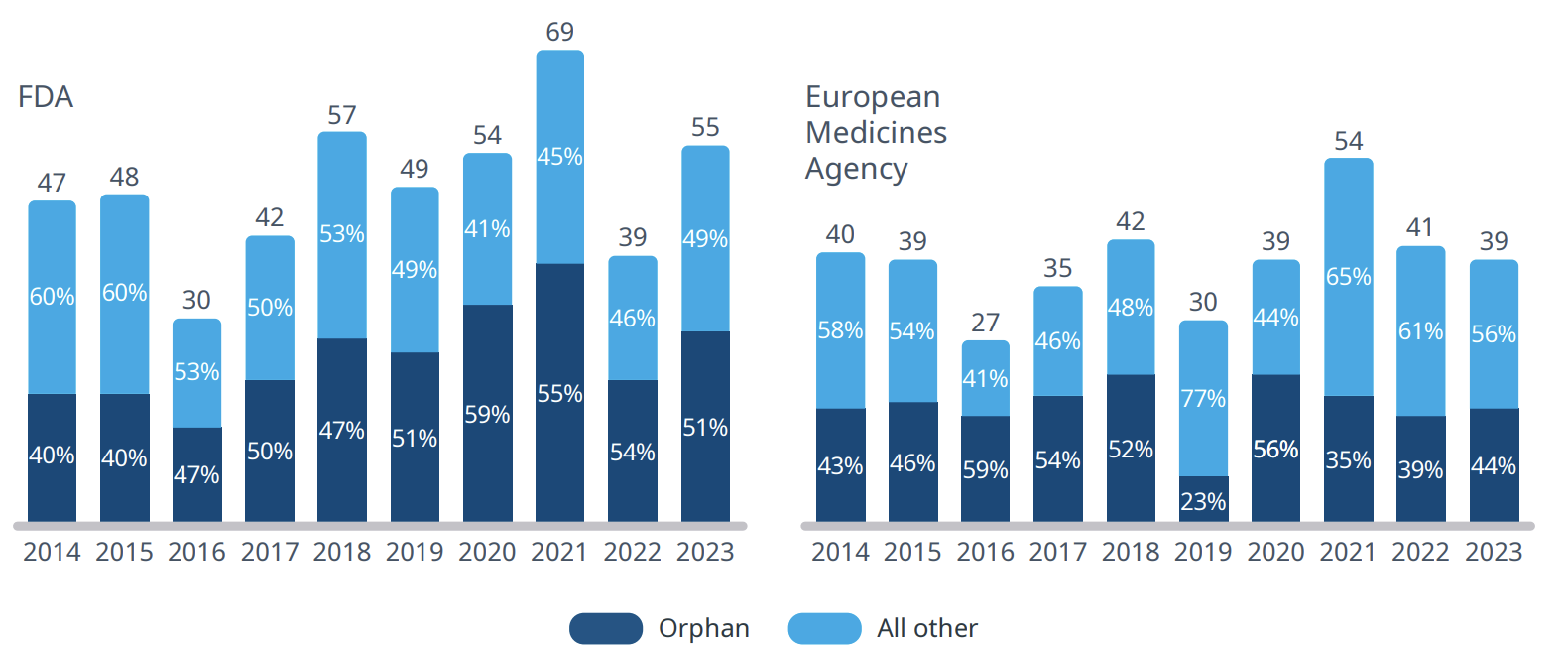
아이큐비아 사라 릭우드(Sarah Rickwood) 부사장은 19일 “최근 승인된 신약 중 희귀질환 타깃 신약이 미국에선 절반가량, 유럽에선 약 45%를 차지했다”면서 “현재 확인된 1만개에 달하는 희귀질환 중 FDA에 승인받은 치료제는 5%에 불과해, 여전히 신약 탄생이 높은 영역”이라고 전했다.
특히 희귀질환 영역에선 신흥 바이오제약 기업의 신약 승인은 글로벌 빅파마 수준에 버금갔다. 2023년 미국에서 29개 신약이 희귀의약품지정으로 출시됐으며, 이 중 14개를 신흥 제약바이오 기업에서 출시했다. 또 같은 해 미국에서 신흥 바이오제약 기업이 출시한 새로운 활성 물질 중 51%가 희귀유전 질환을 타깃하는 것으로 나타났다. 즉, 신흥 바이오제약 기업들은 신약 개발 성공 전략으로 희귀유전 질환을 주 대상으로 삼고 있다.
사라 릭우드 부사장은 “지난해 미국 대형 제약사에서 출시한 제품 3분의 1도 희귀의약품”이라면서도 “대형 제약사는 자체 개발과 함께 희귀질환 전용 프로그램을 통해 유기적으로 신약후보물질을 인수하거나, 무기적으로 회사 전체를 인수하는 방식으로 희귀의약품을 확보했다”고 설명했다. 그럼에도 대형 제약사는 신흥 바이오제약사 보다 희귀질환 타깃에는 집중을 덜 하는 모습이다.
실제 대형 제약사의 희귀질환 타깃 임상시험은 감소세다. 2013년 55%에 달했던 대형 제약사의 희귀질환 타깃 임상시험은 2023년 27%로 급감했다. 반대로 신흥 바이오제약 기업은 2013년 32%에서 2023년 61%로 두 배가량 증가했다.
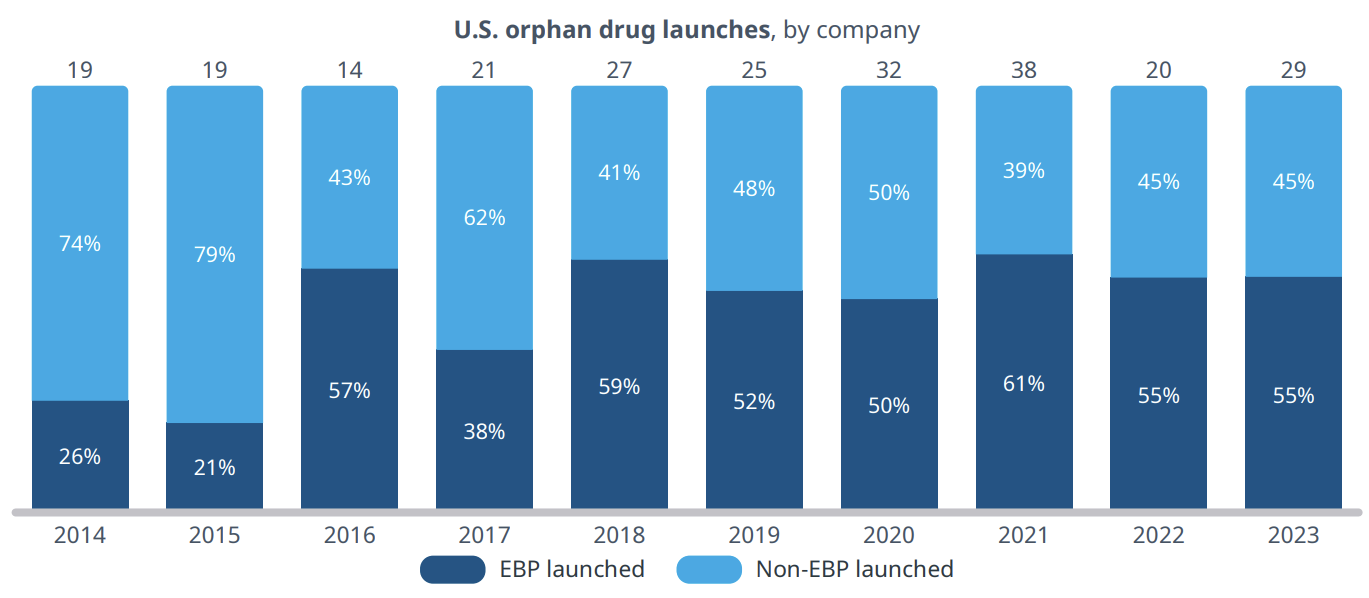
신흥 바이오제약 기업이 미국에서 출시한 희귀의약품은 2014년 26%에서 2016년 57%로 급증 후, 2017년만을 제외하고 2023년까지 50%대를 유지 중이다. 희귀의약품 출시는 최근 5개년 중 2021년이 38건으로 가장 많았고, 2020년 32건, 2019년 25건, 2023년 29건, 2022년 20건 순이다. 대부분 신흥 바이오제약 기업의 희귀의약품 출시 건수가 더 많았다.
사라 릭우드 부사장은 “희귀유전 질환을 중심으로 한 신약개발 전략은 코로나19 팬데믹으로 급변한 의약품 시장의 도전 과제를 극복하고, 희귀유전 질환자에게 새로운 삶을 줄 수 있는 혁신적인 전략이 될 것”이라고 전했다.
한편 프로스트앤설리반(Frost&Sullivan)이 최근 발간한 보고서 ‘Global Orphan Drug Growth Opportunities’에 따르면 2023년 글로벌 희귀의약품 시장 규모는 전년대비 10.8% 증가한 2068억 달러(약 277조353억원)를 기록했다. 이 시장은 향후 5년간 연평균 10.8% 증가해 2028년엔 3458억 달러(약 463조1991억원)만큼 성장할 전망이다.
|
-
01 한국유니온제약 상폐 수순…정리매매 돌입 속... -
02 "공정 불순물 관리 핵심 ‘HCP’ 분석·제어 전... -
03 에피바이오텍, 동종 모유두세포 치료제 핵심... -
04 트럼프,의약품 관세 부과...한국산 의약품 1... -
05 큐라클, CU01 당뇨병성 신증 임상2b상 효능·... -
06 LG화학, 모치다제약 자궁내막증 치료제 ‘디... -
07 [2026 기대 신약 TOP 10] ② 비만 치료제 '올... -
08 [영상] KOREA PACK & ICPI WEEK 2026, 제조 ... -
09 깐깐해지는 의약품 제조 규제… 제약 제조 혁... -
10 [최기자의 약업위키] 자궁내막암 면역항암제...











