뉴스
식약처, 골다공증치료제 37품목 '급성신부전증' 이상반응 추가
'이반드론산나트륨일수화물' 성분 시판후 보고, 피해구제 급여도 지급
김용주 기자 │ yjkim@yakup.com


입력 2019-07-10 12:00 수정 2019.07.10 13:09
골다공증치료제인 '이반드론산나트륨일수화물' 성분 의약품이 시판후 사용중 이상반응으로 '급성신부전중'이 보고돼 허가사항이 변경된다.
식품의약품안전처는 골다공증치료제인 '이반드론산나트륨일수화물'이 시판후 사용중 중대한 이상사례로 '급성신부전'이 발생해 국내 국내 부작용 피해구제 급여를 지급한 사례가 있다며 이상반응을 허가사항에 반영할 예정이라고 10일 밝혔다.
또 식약처는 골다공증치료제인'이반드론산나트륨일수화물'이 시판후 사용중 중대한 이상사례는 이미 국외 허가사항(미국)에 반영되어 있다고 덧붙였다.
국내에서 허가받은 '이반드론산나트륨일수화물' 성분 의약품은 37개품목이다.
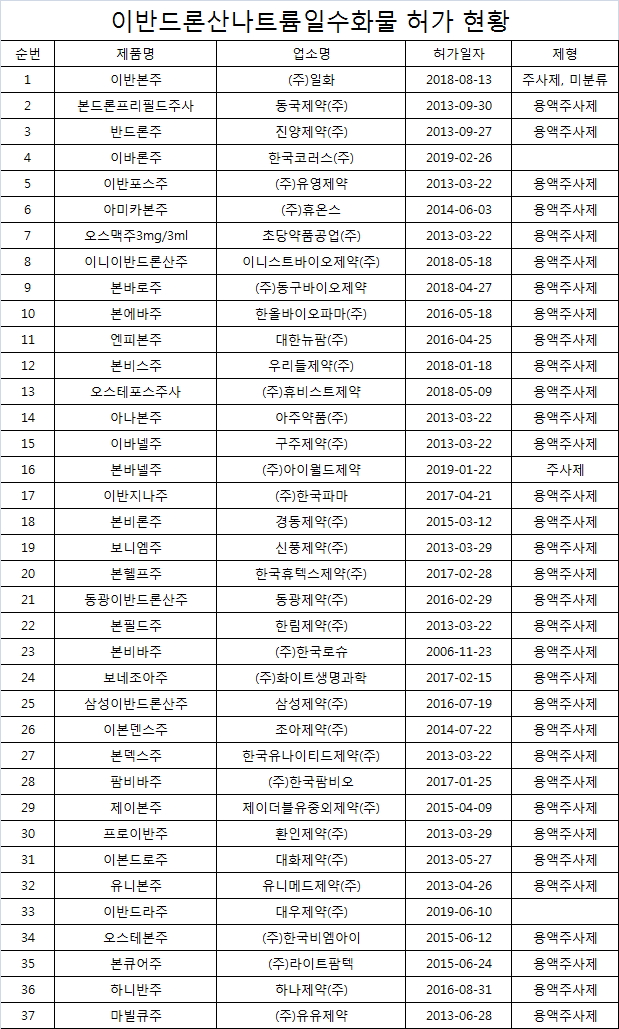
|
전체댓글 0개
등록된 댓글이 없습니다.
오늘의 헤드라인
-
01 바이오포아, 국내 기술 PRRS 생백신 멕시코 ... -
02 유한양행 Ez-PAVE 연구, 글로벌 이상지질혈... -
03 바이오솔루션, 순이익 122억원 늘며 '흑자전환' -
04 한국감사협회, ‘내부감사·컴플라이언스 전문... -
05 GC녹십자, 면역글로불린 내 ‘혈전 유발 불순... -
06 미국 제약협회, 의약품 관세 도입 반대입장 ... -
07 노보 “릴리 ‘파운다요’보다 ‘위고비’ 정제가... -
08 한미약품, 미국암연구학회서 국내 최다 연구... -
09 [약업 분석] 코오롱생명과학, 적자 늪 벗어... -
10 유전자교정협의회 "한국 규제, 글로벌과 불...











